Восстановительное свойство - элемент
Cтраница 1
 |
Физические константы простых веществ ванадия, ниобия и тантала. [1] |
Восстановительные свойства элементов усиливаются с уменьшением атомного радиуса. [2]
Окислительные или восстановительные свойства элемента можно оценить по его стандартному электродному потенциалу. [3]
В результате этого восстановительные свойства элементов подгруппы ПА уменьшаются, а подгруппы ПВ возрастают по сравнению с соответствующими элементами I группы. [4]
 |
Электронное строение, радиусы атомов и ионов элементов. [5] |
Отсюда следует: а) восстановительные свойства элементов в подгруппе IA выше; б) ионизационный потенциал ниже; в) степень металличности элементов подгрупп IA и IB не одинакова. У элементов подгруппы IA заполнены s - и р-подуров ни предвнешнего слоя, а на d - орбиталях электронов нет. Энергетические характеристики электронов внешнего и предвнешнего уровня заметно различаются. У элементов подгруппы IB в предвнешнем уровне заполнены S -, р-и d - орбитали. Радиусы атомов Си, Ag, Аи не на много отличаются от предшествующих элементов, поэтому энергетические характеристики s - состояний внешнего уровня и d - орбиталей предвнешнего в подгруппе IB отличаются незначительно. Как следствие этого, элементы побочной подгруппы IB могут проявлять степень окисления, не только равную 1, но и более высокую. [6]
По мере продвижения в периодах влево восстановительные свойства элементов усиливаются довольно быстро. Сера хорошо горит в кислороде. В еще большей степени это относится к фосфору. [7]
 |
Зависимость значений электроотрицательности ЭО элементов ( черные кружки, первых потенциалов ионизации 1 ( светлые кружки и сродства к электрону ( - J - их атомов от зарядов ядер атомов ( Z. [8] |
В пределах одного периода по мере роста заряда ядра и уменьшения размеров атомов они более прочно удерживают свои электроны, их потенциалы ионизации увеличиваются и восстановительные свойства элементов сменяются окислительными - происходит переход от металлов к неметаллам. Симметричное или полное заполнение электронами подслоев упрочняет электронную оболочку атома, что проявляется в пиковых значениях 1 на представленной зависимости 1 от Z. Это наблюдается у элементов II А-группы ( п 2-заполнение), VA-группы ( ns2np3), II В-группы [ ( - l) d ns2 ] и особенно у элементов VIII А-группы ( ns rap6) - благородных газов. [9]
 |
Положение металлов и неметаллов в периодической. [10] |
В пределах одного периода по мере роста заряда ядра и уменьшения размеров атомов они более прочно удерживают свои электроны, их потенциалы ионизации увеличиваются и восстановительные свойства элементов сменяются окислительными - происходит переход от металлов к неметаллам. Симметричное или полное заполнение электронами подслоев упрочняет электронную оболочку атома, что проявляется в пиковых значениях 1г на представленной зависимости 1г от Z. Это наблюдается у элементов ПА-группы ( гав2 - заполнение), VA-группы ( ns2np3), ПВ-группы [ ( п - I) d10res2 ] и особенно у элементов VIIIA-группы ( ns2npe) - благородных газов. [11]
Как изменяются восстановительные свойства элементов II группы главной подгруппы по мере возрастания порядкового номера элемента и почему. [12]
 |
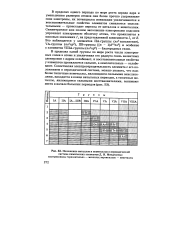
Ионизационные потенциалы лития, бериллия и бора, в.| Зависимость значений ионизационных потенциалов ( 1 элементов от их порядкового номера ( Z. [13] |
В точках максимума на кривой расположены благородные газы, самые слабые восстановители, а в точках минимума - атомы щелочных металлов, наиболее сильные восстановители. Таким образом, восстановительные свойства элементов изменяются периодически. [14]
Радиусы атомов элементов этой подгруппы меньше радиусов атомов подгруппы титана и мало изменяются от ванадия к танталу. Как следствие этого - восстановительные свойства элементов ниже, чем в подгруппе титана; связь с электроотрицательными элементами ( О, С1) близка к ковалентной. [15]
Страницы: 1 2