Другое свойство - кристалл
Cтраница 1
Другое свойство кристаллов, зависящее от наличия водородных связей, - это твердость. Поскольку межмолекулярные силы между соседними органическими молекулами обычно невелики и отличаются от взаимодействия соседних ионов в неорганических ионных соединениях, кристаллы органических веществ, как правило, довольно мягкие. Однако бывают исключения, так, например, кристаллы полигидроксисоединений ( сахара) проявляют исключительную твердость, вероятно за счет образования водородных связей. [1]
Не останавливаясь на других свойствах кристаллов, тепловых и оптических явлениях, которые точно так же объясняются изложенной картиной кристалла как правильно построенной системой электрических зарядов, собранных в атомы и комплексы, рассмотрим еще вопрос об абсолютной величине молекулярных сил. Ограничимся ионными кристаллами, где вопрос решается особенно просто; в качестве примера выберем каменную соль. [2]
Экспериментальные результаты по теплоемкостям и другим свойствам кристаллов в широком интервале температур хорошо описываются набором указанных функций. [3]
С молекулярной точки зрения описанные выше и другие свойства кристаллов могут быть поняты только, если допустить правильное пространственное расположение частиц, из которых состоит кристалл. [4]
Энергетические, оптические, тепловые и некоторые другие свойства кристаллов зависят от энергетического состояния валентных электронов. [5]
Энергия активации находится в тесной связи с другими свойствами кристалла. Она порождается тепловыми колебаниями. Поглощение тепловой энергии выражается не только в увеличении амплитуды колебаний частиц, но и приводит к тому, что атомы или ионы покидают свои нормальные места в решетке. При высоких температурах, когда тепловые колебания достаточно велики, может произойти обмен местами - диффузия. [6]
Дислокации оказывают влияние на электросопротивление, оптические и полупроводниковые, магнитные и другие свойства кристаллов. [7]
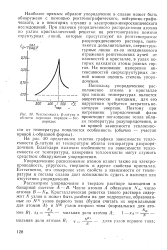 |
Теплоемкость 6-латуни и. [8] |
Упорядоченное расположение атомов влияет также на электропроводность, упругость, твердость и другие свойства кристалла. Естественно, что измерение этих свойств в зависимости от температуры и состава сплава дает возможность судить о наличии или отсутствии упорядочения. [9]
Энергия решетки оказывается очень полезным параметром, который находится в тесной связи с другими свойствами кристаллов. [10]
Нитрат аммония NH4NO3, традиционно но неправильно называемый аммиачной селитрой ( правильнее называть аммонийной селитрой), при атмосферном давлении в интервале от - 50 С до температуры плавления 169 6 С существует в пяти кристаллических формах / - V, различающихся структурой, удельным объемом и другими свойствами кристаллов. На политермической диаграмме системы NH4NO3 - H2O ( рис. 5.1) показаны температурные интервалы стабильности / - IV кристаллических форм. Модификация V стабильна ниже - 16 9 С. [11]
Например, если из кубического кристалла хлорида натрия вырезать два бруска - один перпендикулярно граням куба, другой по диагонали одной из граней - и испытать их на разрыв, то окажется, что для разрыва второго бруска потребуется сила вдвое большая, чем для разрыва первого бруска. Анизотропия проявляется и в других свойствах кристаллов ( теплопроводность, электрическая проводимость, поляризация света и пр. [12]
Характерной особенностью кристаллических тел, вытекающей из их строения, является анизотропия. Она проявляется в том, что механические, электрические и другие свойства кристаллов зависят от направления в кристалле. [13]
 |
Кристаллическая решетка аргона.| Кристаллическая решетка иода. [14] |
Характерной особенностью кристаллических тел, вытекающей из их строения, является анизотропия. Последняя проявляется в том, что механические, электрические и другие свойства кристаллов зависят от направления в кристалле. [15]
Страницы: 1 2