Калорические свойство
Cтраница 3
Как было показано в § 1.1, калорические свойства реальных газов, в том числе теплоемкость и энтальпия, могут быть рассчитаны с помощью дифференциальных уравнений термодинамики, если имеется уравнение состояния в вириальной форме, описывающее с достаточной точностью поведение реальных газов в широком диапазоне изменения термодинамических параметров. Однако даже в этом случае при вычислении теплоемкости необходимо выполнять операцию двойного дифференцирования экспериментальных данных, точность которой невелика, а поэтому вычисленные таким образом значения теплоемкости будут определены с большой погрешностью. [31]
Как будет показано в дальнейшем, существуют и другие калорические свойства. [32]
Представление о молекулах как жестких образованиях правильно описывает калорические свойства одноатомных газов, а для двухатомных газов это представление оказалось удовлетворительным лишь в определенных интервалах температур. Расхождение опыта и теории связано с тем, что при определенных условиях молекулы ведут себя не как жесткие, а как упругие образования, обладающие дополнительными степенями свободы. [33]
Совокупность термического и теплового уравнений состояний позволяет найти различные термические и калорические свойства. [34]
Перечисленными работами исчерпываются все известные нам экспериментальные исследования калорических свойств жидкого аргона. [35]
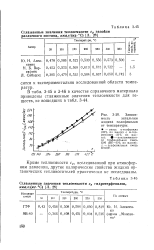 |
Зависимость энтальпии жидких полифенилов от температуры. [36] |
Кроме теплоемкости ср, исследованной при атмосферном давлении, другие калорические свойства жидких органических теплоносителей практически не исследованы. [37]
Рассмотрим пример использования дифференциальных уравнений термодинамики для вычисления некоторых калорических свойств Ван-дер - Ваальсовского газа. [38]
В последние годы опубликовано несколько работ, в которых обобщены калорические свойства щелочных металлов в конденсированной фазе. Однако для повышения надежности рекомендуемых значений необходимо уточнить калорические функции конденсированных щелочных металлов. Такому уточнению способствуют новые экспериментальные работы и более строгий анализ результатов исследований, уже вошедших в существующие обобщения. [39]
В настоящей главе по уравнению состояния ( 84) рассчитаны термические и калорические свойства аргона в интервале температур 85 - 170 К при давлениях до 500 бар. [40]
Разработан, сконструирован, изготовлен и испытан крио-стат для измерения калорических свойств газов и газовых смесей в широком интервале низких температур. В этом аппарате определен эффект Джоуля - Томсона. [41]
Рассмотрим пример - использования дифференциальных уравнений термодинамики для вычисления некоторых калорических свойств Вая-дер - Ваальсовского газа. [42]
Полученные по уравнениям ( 85) - ( 87) значения калорических свойств аргона сопоставлены с указанными выше табличными данными. [43]
Те же подходы, как выясняется, можно использовать и для описания калорических свойств нефтепродуктов. [44]
Такого рода представления помогают создать приближенную ( так называемою классическую) теорию калорических свойств газов. [45]
Страницы: 1 2 3 4