Банановые связи
Cтраница 1
Банановые связи в циклопропановом кольце приводят к увеличению s - характера связи С - Вг, что затрудняет отщепление атома брома в виде аниона. [1]
Модифицированная ь-р 3-гибридизация и банановые связи не являются единственно возможным способом описания характера и свойств связей в циклопропане. [2]
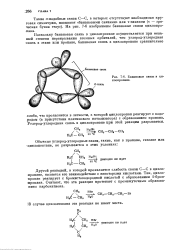 |
Банановые связи в циклопропане. [3] |
На рис. 7 - 6 изображены банановые связи циклопропана. [4]
Нельзя, однако, забывать, что банановые связи не являются ни следствием этого критерия, ни описанием, существенно лучшим, чем картина л - сг-связывания. [5]
Как и у циклопропана, здесь в создании структуры участвуют банановые связи. Водороды СН2 - групп делятся на два типа, напоминающих экзо - и эн3о - положения в производных бицикло [2,2,1] гептана. [6]
Как и у циклопропана, здесь в создании структуры участвуют банановые связи. Водороды СН2 - групп делятся на два типа, напоминающих экзо - и эндо-положения в производных бицикло [2,2,1] гептана. [7]
Отсюда следует, что отдельные валентности кратной связи равноценны и имеют изогнутую форму ( банановые связи), т.е. ни одна из них не проходит вдоль линии кратчайшего расстояния между ядрами обоих атомов. [8]
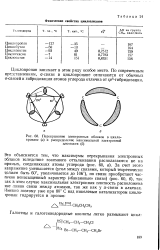 |
Перекрывание электронных облаков в циклопропане ( а и распределение максимальной электронной плотности ( б. [9] |
За счет этого напряжение уменьшается ( угол между связями, который теоретически должен быть 60, увеличивается до 106), но связи приобретают частично ненасыщенный характер ( банановые связи) ( рис. 60, б), так как в этом случае максимальная электронная плотность расположена зне линии связи между атомами, так же как у л-связи в алкенах. [10]
Как и у циклопропана, здесь в создании структуры участвуют банановые связи. [11]
 |
Циклопропан ( по Коулсону, стр. 205. [12] |
С возможностью изменения валентных углов Н - С - Н и С-С - Н связан, по-видимому, некоторый отход от нормального положения, так что плоскость кольца не является уже плоскостью симметрии. В результате этого атомы водорода могут занять расположение в промежутках, подобно нечетной форме ( конформа-ции) этана. Можно сказать, что вместо обычных сосисок здесь имеют место банановые связи, так как при этом достигается наилучшее спаривание. [13]
Переход от структуры 1а к структуре 16 при фиксированном положении молекулы НСООН в плоскости zy ( ср 0) не имеет энергетического барьера и понижает энергию системы на 2 1 кДж / моль. Поворот молекулы Н2О на 90, соответствующий этому переходу, вызывает регибридизацию кислородного атома окисного кольца Oi без изменения заряда на нем. Уменьшаются заселенности одной из НП, ответственной за Н - связь с молекулой Н2О, и валентно активной орбитали 2pv, образующей банановые связи с углеродными атомами цикла. На столько же увеличивается заселенность другой НП, не участвующей в Н - связи и принявшей в структуре 1б вид 2р v-орбнтали. [14]
 |
Перекрывание электронных облаков в циклопропане ( а и распределение максимальной электронной плотности ( б. [15] |
Страницы: 1 2