Симметричные водородные связи
Cтраница 1
Симметричные водородные связи с потенциалом без барьера должны также обладать относительно высокой поляризуемостью, хотя она может быть значительно меньше, чем в случае потенциала с двумя минимумами. Это показывает, что уширение обусловлено поляризуемостью водородной связи. [1]
Такие симметричные водородные связи, функция потенциальной энергии которых имеет два минимума, поляризуются исключительно легко. Эта поляризуемость обусловлена индуцированным дипольным взаимодействием между водородными связями и ионами, взаимодействием между этими водородными связями за счет протонных дисперсионных сил, а также взаимодействием переходов протона в водородных мостиках с низкочастотными колебаниями, и в особенности с межмолекулярными колебаниями. Эти взаимодействия приводят к тому, что энергетические уровни протона размываются в непрерывную полосу, если такие водородные связи существуют в некристаллической среде. В результате для целого ряда систем в ИК-спектрах наблюдается непрерывное поглощение, свидетельствующее о наличии указанных взаимодействий. Высокая поляризуемость таких водородных связей позволяет объяснить механизм аномально большой проводимости, индуцируемой полем. [2]
Встречаются и сильные симметричные водородные связи, приближающиеся по энергии к химическим, как, например, в комплексах ( FHF) -, ( Н502) - 120 - 250 кДж / моль. [3]
Оно обнаруживается также и в неводной среде, когда избыточные протоны образуют между молекулами растворителя симметричные водородные связи, характеризуемые потенциальной функцией с двумя минимумами, как, например, в диметилсульфоксиде или спиртах. [4]
В этих процессах могут играть роль не только симметричные водородные мостики МН - - N с потенциальной кривбй с двумя минимумами, но также и менее симметричные водородные связи, в которых, однако, возможен перенос протона, как это было видно в разд. [5]
Для образования водородной связи А - Н - - - В существует объяснение по методу молекулярных орбиталей в трехцентровом приближении ( см. разд. При этом симметричные водородные связи имеют равномерное распределение электронного облака, а асимметричные связи - повышенную электронную плотность в той части связи, которая короче. [6]
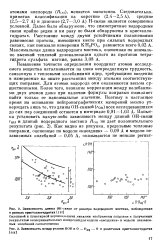 |
Зависимость длины ОН-связи от размера водородного мостика, наблюдаемая в разных кристаллогидратах [ ill ]. [7] |
Следовательно, принятая классификация на короткие ( 2 4 - 2 5 Л), средние ( 2 5 - 2 7 А) и длинные ( 2 7 - 3 0 А) Н - связи является совершенно условной. Далее было обнаружено, что симметричные водородные связи крайне редки и ни разу не были обнаружены в кристаллогидратах. Расстояние между двумя устойчивыми положениями равновесия протона, имеющими место при сильных водородных связях, как показали измерения КН2Р04, равняется всего 0 02 А. Максимальная длина водородного мостика, оцененная по аномально высокой тепловой делокализации одного из протонов тетра-гидрита сульфата магния, равна 3 08 А. [8]
В дальнейшем мы будем предполагать, что в несимметричных связях А - Н - - - В протон локализован в потенциальной яме вблизи атома А. К этому же типу относятся симметричные водородные связи с двумя потенциальными ямами, если высота ( Еа) разделяющего их барьера удовлетворяет неравенству Еа hv0, где v0 - частота протона в изолированной яме. [9]
Сложнее обстоит дело в случае симметричных водородных связей, к вопросу о природе которых существуют два основных подхода. Согласно одному из них, симметричные водородные связи имеют донорно-акцепторный характер и являются, в основном, ковалентными. [10]
Сложнее обстоит дело в случае симметричных водородных связей, к вопросу о природе которых существуют два основных подхода. Согласно одному из них, симметричные водородные связи имеют донорно-акцепторный характер и являются, в основном, ковалентными. Однако функционирование в качестве акцептора требует использования водородом высокого энергетического уровня 2s, что и выдвигалось в качестве решающего возражения против рассматриваемой трактовки. [11]
В дальнейшем мы будем предполагать, что в несимметричных связях А - Н - - - В протон локализован в потенциальной яме вблизи атома А. К этому же типу относятся симметричные водородные связи с двумя потенциальными ямами, если высота ( Еа) разделяющего их барьера удовлетворяет неравенству Еа / ivfl, где v0 - частота протона в изолированной яме. [12]
Каждый атом кислорода связан таким аюсоиом с двумя другими. Эти связи первоначально рассматривались как симметричные водородные связи, но, невидимому, правильнее считать их гидроксильными связями, как по их длине ( 2 71 0 05 А), так и потому, что каждый атом кислород) образует две такие связи. В кислых солях, где имеются короткие водородные связи ( 2, 55 А), каждый атом кислорода образует тольк-одну такую связь ( см. стр. [13]
Остатки гистидина, например, протонируются ( и депротонируются) в физиологическом интервале рН, поэтому они должны образовывать связи, включающие туннельные протоны. Функциональной группой гистидина является имидазоль-ная группа, которая, как мы знаем, в присутствии избыточных протонов образует симметричные водородные связи, включающие туннельные, протоны. [14]
В предыдущих разделах мы видели, что непрерывное поглощение возникает не только тогда, когда протон совершает туннельный переход между молекулами воды, но также и в том случае, когда протоны участвуют в образовании симметричных водородных связей с потенциальной функцией с двумя минимумами. Если величина рКа акцепторной группы молекул, растворенных в воде, больше р / С0 для воды, то при увеличении степени протонирования должны образоваться симметричные водородные связи между растворенными молекулами даже в водном окружении. [15]
Страницы: 1 2