Электростатические связи
Cтраница 1
Электростатические связи этого типа могут быть названы ион-ди-польными связями. Электростатические связи могут быть также обусловлены притяжением между ионом и индуцированным моментом поляризующейся молекулы или взаимным притяжением постоянных диполей двух молекул. [1]
Обнаруживаемые в пеке полярные гетероциклы обусловливают электростатические связи в молекулах и между ними. Действием этих сил может быть объяснено переохлаждение пека как жидкого тела. [2]
При превращении микрогеля в кристаллическое тело ослабляются электростатические связи ионов твердой фазы с ионами адсорбционного и диффузного слоев. В связи с этим уменьшается разность потенциалов ( ЧГ-Ч1 2), одновременно снижается подвижность катионов и анионов ( о о), а вместе с этим и поверхностная проводимость YS - Закономерное ослабление электростатических связей между указанными фазами свидетельствует о том, что процесс стремится к изоэлек-трической точке; она показывает, что адсорбционно связанная жидкость удерживается теперь не электровалентными связями, а силами Ван-дер - Ваальса, возникающими в результате флуктуации электронных оболочек атомов. Эти же силы удерживают ионную среду в жидкой фазе. Указанное адсорбционное явление, обусловливающее образование двойного электрического слоя на нейтральных ( незаряженных) поверхностях, объясняет эффект перезарядки. [3]
Во всех случаях эти точки являются ионными группами, способными образовать электростатические связи с ионами, противоположными по знаку заряда. Легкость, с которой ион вступает в обмен, определяется прочностью связи, которая изменяется подобно энергии диссоциации слабых и сильных электролитов. Закономерности, управляющие обменом ионов в гетерогенных системах, совершенно аналогичны закономерностям, существующим в растворах электролитов. [4]
Как видно, в октаэдрических комплексах железа е фтором и водой преобладают электростатические связи, а в комплексах с цианидными, нитритными и дипиридильными группами - ковалентные3 связи. [5]
Исследование строения дициклопентадиенилкальция при помощи ИК-спектров ( в дальней области) [11] подтверждает сэндвичевую структуру и обнаруживает электростатические связи колец с центральным атомом металла. [6]
Заметим, между прочим, что основное направление провода считывания - вдоль диагонали матрицы - максимально уменьшает электромагнитные и электростатические связи этого провода с горизонтальными и вертикальными проводами выбора. [7]
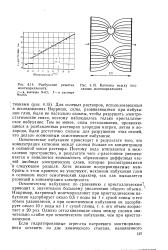 |
Разбухание решетки [ IMAGE ] Катионы между под-монтмориллонита. слоями монтмориллонита / - в растворе N301. 2 - в растворе. [8] |
Для солевых растворов, использовавшихся в исследованиях Норриша, силы, развивающиеся при набухании глин, были не настолько сильны, чтобы разрушить электростатические связи, поэтому наблюдалось только кристаллическое набухание. Тем не менее, силы отталкивания, проявляющиеся в разбавленных растворах хлоридов натрия, лития и водорода, были достаточно сильны для разрушения этих связей, что делало возможным осмотическое набухание. [9]
Силы, определяющие взаимодействие между активными центрами ферментов и молекулами субстрата, которые подвергаются каталитическому процессу, могут быть весьма разнообразны, как-то: химические, ковалентные, электростатические связи, а также водородные связи и ван-дер-ваальсовы силы. [10]
Хаккерман и Макридес [107] отмечают, что катодное ингибирующее действие может быть результатом как физической адсорбции, так и хемосорбции. Электростатические связи на катодных участках способствуют общему ингибирующему действию. Хемо-сорбция ингибитора происходит через образование координационных ковалентных связей с поверхностными атомами металла, в силу чего ингибитор действует как донор электронов, а металл - как их акцептор. Этот механизм объясняет зависимость силы инги-бирующего действия от электронной структуры и растворимости ингибитора, а также от природы заместителя, учитывает роль металла и позволяет получить как положительный, так и отрицательный температурные коэффициенты. Шрам и Берне [109] объясняют влияние солей аминов на поляризацию железных катодов на основании кажущихся изменений поверхности, вызванных адсорбцией аминов на катодных участках. В пределах исследованных ими концентраций выраженная в процентах ингибирующая эффективность каждого амина была линейной функцией от степени покрытия поверхности адсорбированными аминами. Связь между степенью экранирования поверхности и ингибирующим действием оказывается очень различной в зависимости от природы амина. Это позволяет прийти к заключению, что действие аминов не сводится лишь к экранированию отдельных участков поверхности корродирующего металла. [11]
Электростатические связи этого типа могут быть названы ион-ди-польными связями. Электростатические связи могут быть также обусловлены притяжением между ионом и индуцированным моментом поляризующейся молекулы или взаимным притяжением постоянных диполей двух молекул. [12]
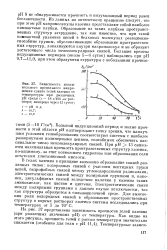 |
Зависимость максимального предельного напряжения сдвига гелей казеина от температуры при различных рН среды ( с 18 г / 100 мл раствора. измерено через 13 суток. [13] |
В гелях казеина в принципе возможно образование связей различных типов: водородных связей с участием пептидных групп цепей, гидрофобных связей между углеводородными радикалами, электростатических связей между полярными группами и, наконец, дисульфидных связей вследствие наличия у казеина таких аминокислот, как цистин и цистеин. Электростатические связи между полярными группами в данном случае исключаются, так как структура образуется в сильнощелочной среде. [14]
Относительно неполярные растворители ( хлороформ, бензол, диэтиловый эфир) разрушают комплексы, образованные гидрофобными взаимодействиями в жировой ткани, хи-ломикроны, комплексы альбумина с жирными кислотами. Полярные растворители ( этанол, метанол) разрушают водородные и электростатические связи. Их применяют в смеси со слабополярными растворителями при экстракции липидов из плазматических мембран, митохондрий, эндоплазматического ретикулума. Липиды, находящиеся в комплексах, образованных ковалентными связями, растворителями не экстрагируются. [15]
Страницы: 1 2