Менее прочные связи
Cтраница 1
Менее прочные связи между цепями ( ван-дер - ваальсовьО могут нарушаться при 1меньших напряжениях; при этом отдельные цепи начинают перемещаться друг относительно друга - проявляется течение. [1]
 |
Строение кристаллов NaCl и РС15 по Косселю. [2] |
Последний имеет более или менее прочные связи внутри молекул, но слабые связи между молекулами, что характерно для типичных кристаллов с молекулярной решеткой. [3]
Между отдельными кружками и революционными группами устанавливаются более или менее прочные связи. [4]
Наряду с основными металлическими связями в процессе схватывания возникают и другие менее прочные связи. [5]
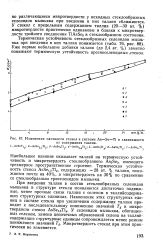 |
Изменение плотности стекол в системе As-Se-Tl в зависимости. [6] |
При введении таллия в состав стеклообразных селенидов мышьяка в структуре стекла ( появляются достаточно подвижные, менее прочные связи таллия с селеном в таллийсодержа-щих структурных единицах. У селенид ов мышьяка, обогащенных селеном, замена цепочечных образований селена на таллий-содержащие структурные единицы сопровождается менее резким понижением значений Tg. Микротвердость стекол, при этом практически не изменяется. [7]
Перекрывание двух л-орбиталей или двух р-орбиталей приводит к образованию прочных ковалеитных связей, но при sp - перекрывании образуются менее прочные связи. Главная причина этого связана со следующим правилом: прочные ковалентные связи образуются при взаимодействии АО примерно одинаковой энергии. [8]
Ионы в реальном кристалле ( мы говорим о ионах только в первом приближении для солей или силикатных систем), которые находятся в непосредственном соседстве со структурными недостатками или дефектами, имеют менее прочные связи, чем масса ионов внутри блока. Поэтому дефекты вблизи ионной поверхности служат в узком смысле слова промоторами электропроводности в твердом веществе; вместе с тем они же служат точками, на которых возможны определенные топохимические реакции ( изложение точки зрения Кольшюттера см. А. Этот чрезвычайно важный принцип химической кинетики был продемонстрирован Хедвал - лем6 на примере сильного окисления сернистого газа на дефектах кварца. Дефектные структуры кварца были специально получены путем полиморфного превращения 5 - - а-кварц; это один из наиболее простых примеров каталитического действия дефектов кристалла. [9]
Учитывая различную прочность связи атомов меди с гидроксильными группами целлюлозы ( возможность частичного замещения ионов меди ионами натрия), можно предположить, что вкомп-лексообразовании могут участвовать не только вторичные, но и, частично, первичные ОН-группы, образующие менее прочные связи с комплексным ионом. [10]
Благодаря прочным связям между молекулами твердые вещества способны сохранять свой объем и форму. Жидкости имеют менее прочные связи между молекулами, ввиду чего они могут сохранять только объем. Газообразные вещества вследствие теплового движения и очень слабой связи между молекулами неспособны самостоятельно сохранять ни форму, ни объем, а всегда занимают все предоставленное им пространство. Нет никакого предела для увеличения объема данной массы газа, если на него не действуют внешние силы или если его расширение не ограничено стенками сосуда. [11]
 |
Структуры решетки NaCl ( а и РС15 ( 6 в свете ионной теории. [12] |
В результате в отличие от тугоплавкого механически прочного ионного кристалла NaCl молекулярный кристалл РС1Г) легкоплавок и непрочен. Он имеет более или менее прочные связи внутри молекул, но слабые связи между молекулами, что характерно для типичных кристаллов с молекулярной решеткой. [13]
 |
Структуры решетки NaCl ( а и РС1Ь ( Ь в свете ионной теории. [14] |
В результате в отличие от тугоплавкого механически прочного ионного кристалла NaCl молекулярный кристалл РС16 легкоплавок и непрочен. Он имеет более или менее прочные связи внутри молекул, но слабые связи между молекулами, что характерно для типичных кристаллов с молекулярной решеткой. [15]
Страницы: 1 2