Свободные связи
Cтраница 1
Свободные связи с плотностью 1019 - 1020 см 3 могут быть полностью заполнены, если содержание Н или F составляет около 0 1 % ( ат. Эксперименты, однако, показывают, что для уменьшения плотности свободных связей необходимы значительно большие количества Н или F. Это свидетельствует о том, что Н и F не всегда наиболее эффективно заполняют свободные связи. [1]
Свободные связи поверхностных атомов насыщены химическими связями загрязнений. Особенно неблагоприятное действие оказывают органические загрязнения. [2]
Если все свободные связи углерода заняты водородом, то Образуется простейший углеводород - метан. В метане каждая рука атома углерода держит по атому водорода. [3]
Примечания: 1 Свободные связи присоединены к атомам, отличным от водорода. [4]
В молекуле этана все свободные связи атомов углерода заняты атомами водорода; такие углеводороды называются предельными или насыщенными. [5]
Присущие атомам различных химических элементов свободные связи принято называть валентностями. Именно числом этих связей ( валентностей) и определяется число атомов, входящих в состав образующихся молекул. Атом водорода имеет одну свободную связь ( одновалентен), при помощи которой он присоединяется к атомам других веществ. Если такой атом присоединяется к атому другого одновалентного вещества, то возникает молекула из двух атомов. Например, атом хлора тоже обладает одиночной свободной связью и образует с атомом водорода молекулу НС1 - вещества, которое в водном растворе носит название соляной кислоты. Если одновалентный атом водорода в этой молекуле заменить одновалентным атомом натрия, то получится молекула NaCl, известная под названием поваренной соли. Атом кислорода имеет две свободные связи ( двухвалентен), почему он при окислении водорода способен присоединить к себе два атома водорода и создать прочную молекулу воды или водяного пара ШО. Гораздо менее прочным соединением окажется так называемая перекись - водорода HjO2, в которой, как понятно, недостаточно погашены свободные связи, присущие кислородным атомам, и потому молекула перекиси оказывается неустойчивой и охотно разваливается на более прочную молекулу воды и активный атом свободного кислорода, вступающий в связь с другим таким же кислородным атомом или каким-нибудь другим достаточно активным веществом. [6]
Ион-атомы на поверхности металла имеют свободные связи, которые могут быть насыщены в результате адсорбции ионов, а также полярных молекул. Валентные электроны покинуть сферу металла в обычных условиях не могут, так как для этого их энергия недостаточна. Выход электронов из металла становится возможным лишь в случае увеличения их энергии, например под влиянием облучения поверхности металла. [7]
 |
Схема электронного строения остатка молекулы этана после отнятия двух атомов водорода. [8] |
В таком случае должны появиться две свободные связи. Очевидно, что характер движения электронов, соответствующих этим валентностям, должен резко измениться, и произойдут глубокие изменения пространственного вида и химического характера молекулы. [9]
Это можно объяснить тем, что свободные связи углерода в различных высокомолекулярных углеводородах обладают неодинаковой способностью к рекомбинации. В кристаллитах кокса ( в связи с их малой подвижностью и стери-ческими затруднениями) - свободные радикалы исчезают медленно, что и обусловливает их повышенный парамагнетизм и реакционную способность. [10]
Это можно объяснить тем, что свободные связи углерода в различных высокомолекулярных углеводородах обладают неодинаковой способностью к рекомбинации. В кристаллитах кокса ( в связи с их малой подвижностью и стери-ческими затруднениями) свободные радикалы исчезают медленно, что и обусловливает их повышенный парамагнетизм и реакционную способность. [11]
У атома углерода карбонильной группы еще остаются две свободные связи. [12]
Другими принципиально отличными методами сварки являются методы, использующие свободные связи по - - верхностных слоев металла. К последним относится холодная сварка с большими пластическими деформациями, сварка сдвигом и сварка ультразвуком. При этих методах нет необходимости в дополнительном вводе тепла в изделие, сварка происходит за счет использования сил межатомного взаимодействия, которые могут при определенных условиях проявить себя путем образования металлических связей на соединяемых поверхностях. [13]
Цементная частица обладает зарядом, если на ее поверхности имеются свободные связи, которые возникают в процессе адсорбции ионов цементной частицей. [14]
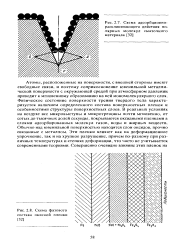 |
Схема адсорбционно-расклинивающего действия полярных молекул смазочного материала.| Схема фазового состава окисной пленки. [15] |
Страницы: 1 2 3 4