Связывание - определяемый ион
Cтраница 1
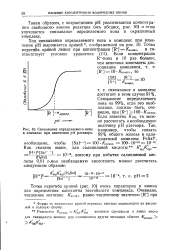 |
Связывание определяемого иона в комплекс при изменении рН раствора. [1] |
Связывание определяемого иона на 99 %, если это необходимо, должно быть, очевидно, ПрИ [ R - ] 100 / Скомпл. [2]
Связывание определяемого иона в комплекс на 99 %, если это необходимо, должно быть, очевидно, при [ К - ] Зг10 ( Жкомпл - Если известна Кип, то можно рассчитать и необходимую величину рН раствора. [3]
Вследствие того что связывание определяемых ионов в окрашенное соединение происходит при некотором избытке реактива, в сравниваемых растворах стремятся создать одинаковые избыточные концентрации реактива. [4]
Методы комплексообразования основаны на связывании определяемых ионов в очень прочные и хорошо растворимые комплексные соединения. В качестве индикаторов при этом применяют обычно органические соединения, образующие с определяемым катионом окрашенные соединения. В настоящее время одним из наиболее распространенных методов этой группы является комплексонометричеокий. Примеры применения этого метода описаны в гл. [5]
Поскольку влияние концентрации реагента в растворе так существенно для связывания определяемого иона, при фотометрических определениях стремятся получить одинаковую концентрацию реагента в измеряемых растворах. [6]
При применении реагентов, являющихся слабыми кислотами, полнота связывания определяемого иона в комплекс возрастает с увеличением рН раствора. Однако при этом необходимо учитывать возможность проявления реагентом индикаторных свойств. Всегда имеется интервал рН, в котором происходит достаточно полное связывание определяемого иона в комплекс, а окраска самого реагента еще не изменяется. [7]
При применении реактивов, являющихся слабыми кислотами, полнота связывания определяемого иона в комплекс возрастает с увеличением рН раствора. Однако при этом необходимо учитывать возможность проявления реактивом индикаторных свойств. Всегда при проведении таких реакций есть интервал рН, в котором происходит достаточно полное связывание определяемого иона в комплекс, а изменения окраски самого реактива еще не происходит. [8]
В связи с тем что концентрация реактива в растворе существенным образом сказывается на степени связывания определяемого иона в окрашенное соединение, при колориметрических определениях стремятся создать одинаковую избыточную концентрацию реактива в сравниваемых растворах. [9]
Ранее было показано, что прочные комплексы имеют значительное преимущество в том отношении, что связывание определяемого иона в такой прочный комплекс не требует большого избытка реактива. [10]
При применении реактивов, являющихся слабыми кислотами, как указывалось в предыдущем разделе, полнота связывания определяемого иона в комплекс возрастает с увеличением рН раствора. Однако при этом необходимо учитывать возможность проявления реактивом индикаторных свойств. Регулировка кислотности раствора при использовании р еакти BOB, о б л а д а ю щи х индикаторными свойствами, имеет первостепенное значение. [11]
Как и в других случаях использования ШС, получению конечного или аналитического продукта реакции предшествует стадия связывания определяемого иона в ГПК. Реакция эта всегда требует избытка лигандч. Успех определения, таким образом, зависит, кроме всего прочего, и от состава комплекса. Специфичность реакции усиливают с помощью нескольких приемов: I) избирательной экстракцией ассоциата ГПК-ОК; 2) применением маскирующих избыточный лиганд веществ; 3) подбором кислотности среды в момент образования конечного продукта. [12]
 |
Связывание определяемого иона в комплекс при изменении рН раствора. [13] |
Таким образом, с повышением рН увеличивается концентрация свободного аниона реактива ( рис. 31) и этим улучшается связывание определяемого иона в поглощающий свет комплекс. [14]
Таким образом, с возрастанием рН увеличивается концентрация свободного аниона реактива ( ось абсцисс, рис. 10) и этим улучшается связывание определяемого иона в окрашенный комплекс. [15]
Страницы: 1 2