Связывание - реагент
Cтраница 2
Конечно, правило селективности, которое исходит только из определенной оптимальной прочности связи кислорода с решеткой в оксидном катализаторе, может не иметь общей значимости. В частности, нельзя ожидать выполнения этого правила при связывании реагента не с кислородом решетки, а с катионом оксида, что принимается для многих каталитических систем. [16]
Мы неплохо представляем себе, как работают ферменты. Природа создает формы молекулярной поверхности, приспособленные для распознавания и связывания определенного реагента. Эта поверхность притягивает молекулы лишь одного типа и удерживает их в определенном положении, благоприятствующем реакции. Когда подходит партнер, сцена уже подготовлена для того, чтобы произошла желаемая реакция с образованием продукта требуемой геометрии. [17]
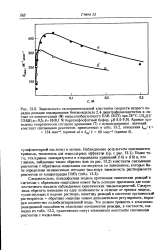
В общем случае зависимость константы связывания ионного реагента от концентрации ПАВ может быть определена в независимом эксперименте. Например, в работе [16] для этой цепи была использована зависимость кажущейся величины рКа ионного реагента ( бензимидазола) от концентрации ЦТАБ. Зависимость рассчитанной таким образом аффективной величины константы связывания анионного реагента ( КА -) от концентрации ПАВ показана на рис. 13.3 В. [18]
Следовательно, псевдофазная модель протекания химических реакций в системах с обратными мицеллами может быть успешно применена для количественного анализа наблюдаемых кинетических закономерностей. Следует лишь обратить внимание на одну особенность: в отличие от прямых мицелл, существующих в водном растворе, кинетику реакций в системах органический растворитель - обратные мицеллы можно дополнительно регулировать, варьирую количество солюбилизированной воды. Это должно привести к изменению реакционной способности отдельных компонентов реакции, в частности, как видно из табл. 13.2, существенно могут измениться константы связывания реагентов с мицеллами. [20]
При десорбции продуктов окисления электроны возвращаются к металлу и в среду попадает нейтральная молекула. Таким образом, электронный обмен является второй функцией активных центров. Если центры образуют связь, достаточно прочную для активирования адсорбата, но недостаточно прочную для образования стабильного комплекса, то тем самым они способствуют связыванию реагентов и промежуточных соединений. [21]
Процесс нитрования, очень важный для промышленности органического синтеза, протекает сложно. Из опыта известно, что нитробензол и другие производные бензола нитруются значительно труднее бензола. Причиной этому в случае нитробензола может быть повышение устойчивости молекулы благодаря уменьшению электронной плотности всех звеньев бензольного кольца под влиянием нитрогруппы. Но возможна и вторая причина, а именно связывание нитрующего реагента ( самой ли азотной кислоты, ее димера или нитрониевого катиона) нитрогруппой в комплекс, что должно мешать действию нитрующего реагента на углеводородные звенья. [22]
Химические исследования, проведенные в последние 20 лет, показали, что пространственные структуры белков необычайно сложны, а формы их молекул имеют решающее значение для осуществления каждым белком его специфической биологической функции. Полипептидная цепь, состоящая из сотен связанных друг с другом аминокислот, принимает такую пространственную форму ( называемую конформацией), которая определяется его аминокислотной последовательностью. Например, молекула коллагена - белка, придающего прочность коже и костям, - имеет форму стержня. Антитела представляют собой молекулы Y-образной формы с выемками, которые служат для распознавания чужеродных веществ и запуска реакций, обеспечивающих их эффективное обезвреживание. Ценная информация об их архитектуре была получена в рентгено-структурных исследованиях. Молекулы ферментов имеют щели, называемые активными центрами, в которых связывание реагентов осуществляется таким образом, что становится возможным образование новых химических связей между ними. Таким образом, определенной биологической функции белка соответствует определенная конформация. Основные успехи в исследовании конфор-мации белков были получены с помощью рентгеновских лучей, а также нейтронных и электронных пучков и других методов, которые позволяют нам как бы увидеть белок под увеличением в миллион раз и более. Выяснение кон-формаций белка показывает, как он выполняет свою биологическую функцию. [23]
Если реакцию проводят при рН 3 - 3 8, то затем при встряхивании хлороформного экстракта с 2 М соляной кислотой комплексное соединение никеля разрушается и никель переходит в водную фазу. В присутствии более 0 1 г никеля на каждые избыточные 250 мг никеля требуется дополнительно вводить по 2 мл раствора реагента. Присутствие меди в количествах вплоть до 25 мг не мешает. Она образует темно-бурый экстрагируемый комплекс, который, однако, разлагается при встряхивании хлороформного экстракта разбавленной соляной кислотой. При увеличении содержания меди уменьшается извлечение кобальта, вероятно, вследствие связывания реагента медью. Кобальт можно количественно извлекать в присутствии 1 г меди, добавив иодид и тиосульфат, однако этот метод не пригоден в присутствии железа, которое затем восстанавливается до Fe ( II) и мешает определению кобальта. Содержание аммонийных солей не должно превышать 1 г, так как в противном случае извлечение кобальта несколько снижается. [24]
Страницы: 1 2