Связывание - углеводород
Cтраница 1
Связывание углеводородов определяется не только их размерами, но и пространственным строением, а также природой гидрофобных областей. Наглядное доказательство этого можно получить, проанализировав данные по связыванию различных углеводородов у-глобулином и сывороточным альбумином. Так, молекулы изопропилбензола, имеющие приблизительно равные объемы с гептаном, связываются белками различно, а связывание гептана и толуола одинаково, хотя объем молекулы гептана больше молекулярного объема толуола. В то же время молекулы циклогексана и толуола, имеющие одинаковые молекулярные объемы и, по-видимому, сходное пространственное строение, связываются - глобулином и сывороточным альбумином в равных количествах. [1]
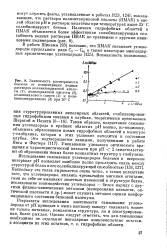 |
Зависимость растворимости бензола от концентрации водных растворов полиметакриловой кисло-ты ( 1, полиакриловой кислоты ( 2, поливинилового спирта ( 3 и поли-винилпирролидона ( 4 при 20 С 0 1. [2] |
Результаты исследования зависимости связывания углеводорода от рН приводят к очень важному выводу: связывать может не только нативная, компактная структура, но и денатурированная, более рыхлая. Однако следует отметить, что для связывания необходимы не отдельные неполярные аминокислотные остатки, а ассоциаты из этих остатков, т, е, гидрофобные области. [3]
 |
Зависимость растворимости бензола от концентрации водных растворов полиметакриловой кисло-ты ( 1, полиакриловой кислоты ( 2, поливинилового спирта ( 3 и поли-винилпирролидона ( 4 при 20 С 0 1. [4] |
Таким образом, возрастание связывания углеводорода в крайних областях рН можно, по-видимому, объяснить образованием новых гидрофобных областей в молекуле Т - глобулина, которая в этих условиях находится в состоянии клубка. Уменьшение удельного оптического вращения и характеристической вязкости при рН 2 свидетельствуют об образовании новых более компактных структур у-глобулина. [5]
Таким образом, при связывании углеводородов глобулярными белками в водных растворах температура денатурации возрастает на 4 - 10, а энтальпия денатурации увеличивается на 2 - 10 ккал / молъ. Повышение термостабильности глобул белка зависит как от степени заполнения гидрофобных областей молекулами углеводородов, так и от природы углеводорода и связывающей неполярной области. [6]
Полученные величины АН показывают, что связывание углеводородов белками приводит % увеличению теплоты денатурации или, что то же самое, к повышению устойчивости нативной глобулярной конформации белка по отношению к денатурации теплом. При этом связывание у-глобулином гептана увеличивает теплоту денатурации на 10 ккал / молъ ( от 55 до 65 ккал / молъ), связывание декана и тетрадекана - от 55 до 57 ккал / молъ. Этот факт очень хорошо объясняется особенностями заполнения глобул белка этими углеводородами, что будет рассмотрено ниже. [8]
Основные результаты исследования солюбилизации углеводородов белками ( связывание углеводородов определяется, во-первых, существованием в макромолекулах неполярных областей, во-вторых, молекулярными размерами углеводородов) выявили возможность оценки емкости гидрофобных областей и распределения их в макромолекулах белков. [9]
 |
Связывание углеводородов ( ЛГ, моль / моль в растворах а-химотрипсина ( 1, рН 4 25 и трипсина ( 2, рН 3 75. с 0 5 г / 100 мл. [10] |
Данные табл. 6 - 8 показывают, что связывание углеводородов белками практически не меняется в интервале 15 - 30 С. Неизменность связывания в этом интервале температур свидетельствует о неизменности состояния гидрофобных областей белков в данных условиях. При понижении температуры ниже 15 и повышении выше 30 С для алифатических углеводородов наблюдается уменьшение связывания. [11]
Конформация белковых молекул оказывает решающее влияние на величину связывания углеводорода. [12]
Установлено, что солюбилизация обусловлена глобулярным состоянием желатины в растворе. Наибольшее связывание углеводорода наблюдается в изоэлектричеоком состоянии. [13]
Рассмотрим результаты определения связывания углеводородов белками при разных температурах. [14]
 |
Содюбилизация углеводородов глобулярными белками. [15] |
Страницы: 1 2
