Связывание - азот - воздух
Cтраница 1
Связывание азота воздуха, которое на полимерных катализаторах можно будет, по примеру некоторых бактерий, легко проводить при комнатной температуре и обычном давлении, раз и навсегда решит проблему азотных удобрений. [1]
При связывании азота воздуха клубеньковыми и свободноживущими азотфик-сирующими бактериями первичным продуктом является А. Выделяемый животными или образовавшийся в результате аммонификации и азотфиксации А. [2]
Первый завод для связывания азота воздуха с по - - мощью электричества был построен в 1902 г. у Ниагарского водопада. [3]
Эта реакция является одним из способов связывания азота воздуха. [4]
Эта реакция является весьма важным способом связывания азота воздуха. [5]
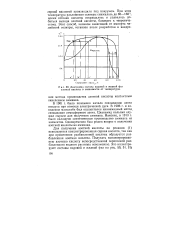 |
Диаграмма состава паровой и жидкой фаз азотной кислоты в зависимости от температуры. [6] |
В 1901 г. было положено начало связыванию азота воздуха при помощи электрической дуги. В 1906 г. в заводском масштабе был осуществлен цианамидныи метод, связывания атмосферного азота. Цианамид кальция служил сырьем для получения аммиака. Наконец, в 1913 г. было налажено синтетическое производство аммиака из элементов. Одновременно был решен вопрос о получении азотной кислоты из аммиака. [7]
Синтез аммиака в заводских условиях осуществляется путем связывания азота воздуха с использованием катализаторов, в качестве которых берется смесь Fe и Fe2O3 с небольшой добавкой А12О3 и КОН, и является очень важным методом промышленного получения азотной кислоты и других азотных соединений. [8]
В настоящее время применяют высокотемпературные плазмо-химические процессы, например связывание азота воздуха и получение ацетилена из метана. [9]
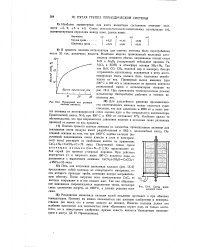 |
Примерный ход реакции синтеза аммиака.| Схема циан-амидной печи. [10] |
Помимо прямого синтеза аммиака из элементов, промышленное значение для связывания азота воздуха имеет разработанный в 1905 г. цианамидный метод. Последний основан на том, что при 1000 С карбид кальция ( получаемый накаливанием смеси извести и угля в электрической печи) реагирует со свободным азотом по уравнению: CaC2 N2CaCN2 C 70 / скал. [11]
 |
Примерный ход реакции синтеза аммиака.| Схема циан. [12] |
Помимо прямого синтеза аммиака из элементов, некоторое промышленное значение для связывания азота воздуха имеет разработанный в 1905 г. цианамидный метод. Последний основан на том, что при 1000 С карбид кальция ( получаемый накаливанием смеси извести и угля в электрической печи) реагирует со свободным азотом по уравнению: СаС2 N2 CaCN2 С 70 ккал. Полученный таким путем цианамид кальция ( Са N - С N) представляет собой серый ( от примеси углерода) порошок. С) водяного пара он разлагается с выделением аммиака: CaCN2 ЗН2О СаСОз 2МНз 53 ккал. [13]
Помимо прямого синтеза аммиака из элементов, некоторое промышленное значение для связывания азота воздуха имеет цианамидный метод. Последний основан на том, что при 1000 С карбид кальция ( получаемый накаливанием смеси извести и угля в электрической печи) реагирует со свободным азотом по уравнению: СаС2 N2 СаСМз С. Полученный таким путем цианамид кальция ( Ca N-C N) представляет собой серый ( от примеси углерода) порошок. [14]
Менее богатая водными силами Германия уделила незначительное место в азотной промышленности связыванию азота воздуха посредством электрической дуги. В 1915 году был основан Завод в Чорневитце. [15]
Страницы: 1 2