Связь - анион
Cтраница 1
Связь анионов с металлом может изменяться во времени. [1]
Однако природа связи анионов с волокнами целлюлозы до сих пор остается не выясненной. Адсорбция некоторых анионных красителей объяснялась иногда образованием водородных связей между гидроксильными группами целлюлозы и такими группами, как амино -, гидрокси - и этокси-группы красителей. При этом в качестве обоснования предположения об образовании водородной связи приводится величина теплоты адсорбции анионов ( 5 ккал. [2]
Однако природа связи анионов с волокнами целлюлозы до сих пор остается не выясненной. Адсорбция некоторых анионных красителей объяснялась иногда образованием водородных связей между гидроксильными группами целлюлозы и такими группами, как амино -, гидрокси-и этокси-группы красителей. При этом в качестве обоснования предположения об образовании водородной связи приводится величина теплоты адсорбции анионов ( 5 ккал. [3]
Механизм Гудинафа учитывает одновременное образование частичных связей аниона с обоими противолежащими катионами. Если спины катионов параллельны, то образование таких связей невозможно. Таким образом, все три механизма ( каждый Б отдельности) дают суммарную антиферромагнитную связь. [4]
Сильно сказывается влияние ДМСО на характер связей анионов, обладающих слабыми электрондонорными свойствами. [5]
Эта же геометрия осуществляется при образовании связи аниона ВзШс медью и хромом. [6]
Замена одного основного окисла другим влияет на энергию связи аниона кислорода со шлаком и на прочность комплексных анионов. Поэтому введение СаО вместо FeO, с одной стороны, должно способствовать сдвигу равновесия, например ( V38), вправо. [7]
 |
Зависимость степени гидролиза галогенид-форм сильноосновных анионитов от энергии гидратации и поляризуемости насыщающих ионов. [8] |
Это приводит к образованию ионных пар Е ], что способствует усилению прочности связи аниона с анионитом и уменьшению степени гидролиза последнего. [9]
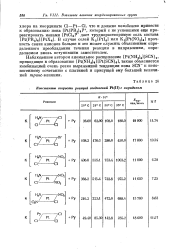 |
Константы скорости реакций соединений Pt ( II с пиридином. [10] |
В случае солей K2 [ PtIJ или K2 [ Pt ( N02) 4 ] прочность связи анионов больше и это может служить объяснением определенного преобладания течения реакции в направлении, определяемом вновь вступившим заместителем. [11]
В случае солей K2 [ PtI4 ] или K2 [ Pt ( N02) 4 ] прочность связи анионов больше и это может служить объяснением определенного преобладания течения реакции в направлении, определяемом вновь вступившим заместителем. [12]
Анионы различных фосфатов, введенные в колонку, заполненную анионообменной смолой в хло-ридной форме, вследствие существующей селективности связи анионов с анионитом адсорбируются и удерживаются анионито-вой смолой, так как анионы фосфатов образуют более прочную связь, чем анионы хлора. [13]
 |
Кинетика обмена анионов Br -, Для случая обмена анионов. [14] |
Для палладия ( рис. 6) показано, что при возрастании потенциала от - 0 05 до 0 54 в связь анионов) Вг - с поверхностью палладия упрочняется. При этом на поверхности палладия отсутствует адсорбированный кислород, следовательно, упрочнение связи обусловлено большим приближением к поверхности металла за счет заряда, как в аналогичных случаях на платине и родии. Влияние кислорода можно объяснить тем, что он адсорбируется на тех местах поверхности, на которых должны адсорбироваться из раствора анионы Вг - при осуществлении акта обмена. Конкурентная борьба между атомами кислорода и анионами брома за места на поверхности металла затрудняет протекание процессов обмена и адсорбции. [15]
Страницы: 1 2 3 4