Связь - молекула
Cтраница 1
Связь молекул с поверхностью слюды носит донорный характер вследствие донорно-акцепторных переходов электронов между молекулами взаимодействующих фаз. В результате адсорбции происходит частичное заполнение электронами интегральных энергетических уровней положительно заряженных дефектов-ловушек и уменьшение эмиссии с гидрати-рованных сколов мусковита. Отражая сложную дефектную структуру поверхности, молекулы воды усиливают электрический рельеф скола слюды. Домены гидратации представляют собой мощные положительно заряженные источники микрополей, обладающие значительным дальнодействием. Они индуцируют отрицательно заряженные центры, рассредоточенные на всей остальной поверхности. [1]
Связь молекул обусловливает различную подвижность макромолекул относительно друг друга, их гибкость. Это определяет такие свойства вещества, как упругость, эластичность, твердость, температуру размягчения, плавления, стеклования. [2]
Связь молекулы с ее соседями учитывается только реактивным полем R, которое, будучи параллельным направлению дипольного момента рассматриваемой молекулы, нисколько не мешает ее вращению. [3]
 |
Термическая темповая десорбция и фото-десорбцня СО с NiSO4 ( стрелками отмечены периоды освещения искрой кадмия. [4] |
Однако связь молекулы с поверхностью не должна быть слишком прочной и минимум потенциальной энергии слишком глубоким, так как, во-первых, потребный квант оказался бы в вакуумной ультрафиолетовой области, а, во-вторых, прочная связь с поверхностью благоприятствует отдаче энергии электронного возбуждения твердому телу. Действительно, приведенная упрощенная картина потенциальных кривых не учитывает отвода энергии адсорбированной молекулы твердым телом. [5]
Поскольку кислород-водородная связь молекулы третичного бутилового спирта на 8 ккал / молъ прочнее, чем углерод-водородная связь в молекуле метана, то легко понять, почему свободные / ирет. [6]
Энергия связи молекулы - это та энергия, которую нужно затратить, чтобы разделить ее на отдельные атомы. [7]
Энергия связи молекулы F2 равна 159 6 кДж / моль. Ниже 55 К имеет кубическую решетку с периодом а 0 667 нм. [8]
Энергии связи молекул Н2, О2, С12 соответственно равны 430, 495 и 240 кДж / моль. [9]
Энергия связей молекул в ассоциатах незначительная, поэтому они весьма неустойчивы и легко разрушаются механическим путем и при повышении температуры. [10]
С связей молекулы сульфида может несколько изменяться ( примерно на 20 - 30) в зависимости от длины и строения алкильного радикала. [11]
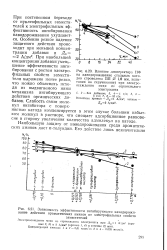 |
Зависимость эффективности ингибирующего наводорожи-вание действия ароматических аминов от электрофильяых свойств. [12] |
Слабость связи молекул ингибитора с поверхностью катода компенсируется в этом случае большим избытком молекул в растворе, что смещает адсорбционное равновесие в сторону увеличения количества адмолекул на катоде. [13]
Уменьшение связи молекул белка с растворителем способствует стабилизации, так как наибольшая устойчивость белковой молекулы характеризуется ее наименьшей сольватацией. [14]
Прочность связи молекулы риванола с остатком цианурхлорида также достаточно велика, и эта связь вполне устойчива к гидролизу. [15]
Страницы: 1 2 3 4