Связь - скорость - реакция
Cтраница 1
Связь скорости реакции с активностями или молярными концентрациями реагирующих веществ выражает порядок реакции. [1]
Связь скорости реакции окисления и ее направления со скоростью движения воздуха в колонне ( иначе говоря, с концентрацией кислорода) не зависит от состава окисляемых фракций керосина. [2]
Методы первого направления устанавливают связь скорости реакции с молекулярными характеристиками исходных веществ и переходного ( активированного) комплекса. При этом сначала строятся модели молекул, как систем с конечным числом электронов, после чего результаты моделирования обобщаются на бесконечные или полубесконечные кристаллы. [3]
Так, например, в работе [148] определена связь скорости реакции разглинизирующего раствора соляной кислоты со степенью карбонатности самого коллектора, из чего следует вывод об уменьшении эффективности разглинизации в таких коллекторах. Поэтому не следует переносить опыт кислотных обработок с одних месторождений на другие, не внося корректировок на особенности химического и минералогического состава пород-коллекторов. Даже в пределах одного месторождения различные залежи и участки следует обрабатывать с учетом особенностей породы-коллектора. Так, например, проведенными исследованиями [544] показано, что распространение монтмориллонита и каолинита по телу пласта Талинского месторождения неравномерно. [4]
В первом разделе настоящей главы был уже указан путь, по которому устанавливается связь скорости реакции с молекулярными характеристиками исходных веществ и переходного ( активированного) комплекса. Метод активированного комплекса позволяет, в принципе, рассчитать константу скорости химической реакции. Однако практически при решении данной задачи возникают значительные трудности, которые препятствуют расчету поверхностей потенциальной энергии с точностью, достаточной для предсказания скорости реакции. [5]
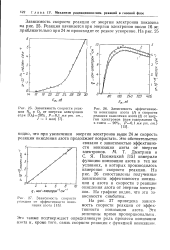 |
Зависимость скорости реак.| Зависимость эффективности ионизации азота ( 1 и скорости реакции окисления азота ( 2 от энергии электронов ( при содержании О2 в смеси - 20 %, Р0 1 мм рт. ст.. [6] |
Это также подтверждает определяющую роль процесса ионизации азота и, кроме того, связь скорости реакции с функцией ионизации. [7]
Отметив, что исследование стерически затрудненных реакций является частью задачи, цель которой - установить связь скорости реакции и строения молекулы, автор показал непродуктивность прямого измерения констант скоростей реакций. Эти константы представляют собой функции многих переменных, из которых основными являются: энергия активации ( Е или д) и константа действия ( предэкспоненциальный множитель) а. Причем каждое из переменных особым образом зависит от строения молекул [ 298, стр. [8]
Такой безбарьерный разряд имеет ряд особенностей как в отношении характера зависимости тока от потенциала, так и в отношении связи скорости реакции с составом раствора. [9]
Такой безбарьерный разряд имеет ряд особенностей как в отношении характера зависимости тока от потенциала, так и в отношении связи скорости реакции с составом раствора. [10]
Уже первая попытка найти корреляцию наблюдаемой константы скорости с диэлектрической проницаемостью среды на примере реакции анилина с бензоилхлоридом, выполненная по данным различных авторов [99], показывает неправомочность рассмотрения связи скорости реакции с природой растворителя с чисто электростатических позиций. Это вполне правдоподобное значение, однако следует отметить, что оно получено из данных для растворителей, которые нельзя отнести к абсолютно инертным по отношению к реагентам. Так, не исключена возможность комплексообра-зования анилина с галогенобензолами за счет образования слабой связи типа водородной. Это значение следует считать весьма и весьма приближенным. От линейной зависимости, построенной в основном по данным для ароматических растворителей ( хлорбензол, нитробензол и некоторые смеси с бензолом), по наклону которой рассчитан цхф, отклоняются данные для бензола ( на 6 порядков. [11]
Характерной чертой окисления углеводородов на полупроводниках СшО и У20б и на металлическом Ag является возможность подавления реакции полного окисления путем увеличения работы выхода электрона. Такую связь скорости реакции образования СО 2 и Аф, вероятно, можно объяснить близостью механизмов этой реакции на различных катализаторах. По-видимому, большую роль в образовании СО а играют цепные процессы на поверхности. [12]
Особенно важно знать влияние среды в поликонденсационных процессах при рассмотрении закономерностей реакций с участием олигомерных исходных продуктов различного молекулярного веса. Полимеризация таких соединений, осуществляемая по реакции с участием концевых функциональных групп, обычно протекает не в растворе, а в массе олигомера, который является в данном случае своеобразным растворителем. Следовательно, в первую очередь нужно найти связь скорости реакции с молекулярным весом олигомера, так как соотношение между концентрацией концевых групп и количеством мономерных звеньев в олигомере, ответственном за свойства среды, является функцией длины цепи олигомера. [13]
Сведения о скорости химической реакции и об энергии активации обычно получают, экспериментально изучая химическую кинетику. В настоящее время все большее значение приобретают работы, посвященные возможностям расчета абсолютной скорости реакции, исходя непосредственно из свойств взаимодействующих молекул. Особый интерес представляет изучение связи скорости реакции с формой потенциальной поверхности. Идея такой связи принадлежит Эйрингу и Поляньи, предложившим в 1935 г. метод активированного комплекса. Допустим, атом С взаимодействует с двухатомной молекулой АВ по реакции АВ С А ВС. По мере приближения С к АВ вдоль прямой, соединяющей ядра А и В, связь между В и С усиливается, а между А и В ослабевает. На некотором расстоянии С от АВ возникает промежуточное состояние, при котором образуется так называемый комплекс А - В - С. При распаде последнего образуется свободный атом А и молекула АС. [14]
Страницы: 1