Связь - водород
Cтраница 3
В той же последовательности прочность связи водорода уменьшается. [31]
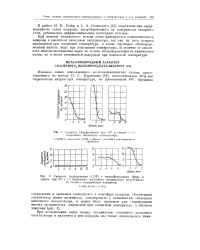 |
Скорость гидрирования при 20 в спирте с 1 г скелетного железного катализатора. [32] |
Рогинского [ 12J энергетическая неравноценность связи водорода, адсорбированного на поверхности сахарного угля, установлена дифференциальным изотопным методом. [33]
Далее оказывается, что энергии связей водорода и углерода с разными металлами различаются между собой, но обычно не более чем на 5 ккал. Для азота эта разница составляет 7 ккал, а для кислорода еще больше, 13 6 ккал. Это может показаться мало, и данный факт можно попытаться объяснить тем, что на разных металлах из набора участков различной активности сама реакция выбирает оптимальные, которые обладают близкими свойствами. Однако к такому заключению следует относиться с осторожностью, так как в дублете участвует 4 реагирующих атома, а разница в 5 ккал, умноженная на 4, дает 20 ккал, что уже составляет большую величину. Вопрос требует дальнейшего изучения. [34]
Симбатная зависимость между величинами энергий связи водорода с катализатором ( УН-К и магнитной восприимчивостью ионов в окислах переходных металлов наблюдалась нами на большом экспериментальном материале - рис. 1 и таблица, в которой для сравнения приведены данные и для других окислов. Для энергии связи Qс - ж - наблюдается антибатная зависимость от и. [35]
Эта энергия значительно превышает энергию связи водорода в молекуле, составляющую 4 5 эв. Поэтому вновь образованный атом дейтерия не остается в молекуле и, обладая большим запасом энергии, должен представлять собой не только активную частицу, но также частицу, способную активировать сталкивающиеся с нею молекулы. [36]
 |
Влияние кислорода в железе на растворимость в нем водорода. [37] |
При сварке сталей металлургические средства обеспечивают связь водорода в газовой фазе с кислородом и фтором в термически прочные нерастворимые в металле газообразные соединения ОН и HF. Соединение кислорода с водородом наиболее полно реализуется при сварке в углекислом газе. [38]
Здесь рассматриваются данные, характеризующие энергию связей водорода с различными элементами и его диссоциации, а также данные о теплотах испарения, конверсии, сгорания и теплопроизводительности. [39]
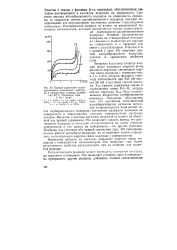 |
Кривые заряжения палла-дированного платинового электрода в присутствии хлорида кадмия при 20 С. Плотность тока 5 - Ю-4 А / см2. [40] |
Нанесение металла на носитель повышает энергию связи водорода с поверхностью катализаторов. Это позволяет еще более регулировать свойства катализаторов при их подборе для заданной реакции. [41]
В-третьих, оказывается, что энергии связи водорода, углерода и кислорода изменяются параллельно магнитному моменту соответствующих редкоземельных элементов ( рис. 33), и это является особенно важным свидетельством в пользу реальности энергий связей, вычисленных при помощи энергетических уравнений мультиплетной теории. [42]
В-третьих, оказывается, что энергии связи водорода, углерода и кислорода с катализатором изменяются параллельно магнитному моменту и. [43]
Эти закономерности объясняются тем, что энергия связи водорода с первичным, вторичным и третичным атомами углерода неодинакова: она составляет соответственно 99, 94 и 90 ккал / моль. Поэтому при галоидировании с большей скоростью замещается водород при третичном атоме углерода. [44]
Первая из них связана с деформационными колебаниями связи водорода в группе - СНС [34] и отсутствует у антисимметричных дизамещенных этилена. Вторая полоса обусловлена неплоскими деформационными колебаниями связей водорода в группе СН2 и характерна для обоих типов связей. [45]
Страницы: 1 2 3 4