Связь - фермент
Cтраница 1
Связь фермента с НАД обусловлена его взаимод. [1]
Поскольку прочность связи фермента с мембранами уменьшается при закислении среды, иммобилизацию фермента в данной серии экспериментов проводят при рН 7 0; содержание фермента в пробе составляет 5 инт. [2]
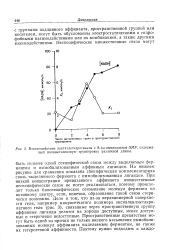 |
Взаимодействие лактатдегидрогеназы с 8 - ( в-аминоадкил - АМР, содержащей полиметиленовую группировку различной длины. [3] |
На нижнем рисунке для сравнения показана специфическая комплементарная связь выделяемого фермента с иммобилизованным лигандом. При низкой концентрации привязанного аффинанта множественные неспецифические связи не могут реализоваться, поэтому происходит только биоспецифическое связывание молекул фермента по активному центру, если, конечно, образование такой связи стери-чески возможно. Дело в том, что из-за неравномерной поверхности геля, например макросетчатого полимера оксиалкилметакри-латного геля ( рис. 3), связанные через пространственную группу аффинные лиганды делятся на хорошо доступные, менее доступные и стеричеоки недоступные. Пространственные препятствия могут быть одной из причин не только низкого насыщения иммобилизованных молекул аффинанта выделяемым ферментом, но также их гетерогенной аффинности. [4]
Кроме того, на стабильность гликозидной связи может влиять природа связи фермента с субстратом. Аналогичным образом изменение электронной плотности у С2 и С8, вызванное чисто химическими факторами ( введением заместителей в кольцо), может вести к облегчению атаки на эти центры, как, например, при ферментативном окислении аде-нина и гуанина до мочевой кислоты. [5]
Роль ионов металлов может быть различной в зависимости от их влияния на прочность связи фермента с молекулой субстрата или на активацию субстрата в промежуточном активном комплексе. [6]
Необходимо отметить, что в образовании фермент-субстратного комплекса участвует несколько функциональных групп фермента, но только некоторые пары из них ( субстрата и фермента) ответственны за ферментативный катализ, а другие группы служат для создания связи фермента с субстратом. [7]
Для открытия гликозидов предложен способ, имеющий почти общее применение. Большую часть природных гликозидов составляют [ - производные глюкозы, которые расщепляются под влиянием специфически действующего на 3-гликозид ную связь фермента эмульсина. Все подобные гликозиды имеют в водных растворах левое вращение, в то время как глюкоза, образующаяся в результате расщепления, обладает редуцирующими свойствами и вращает вправо. [8]
Ион металла может участвовать в ферментативной реакции, не оказывая существенного влияния на прочность связи фермент-субстрат. В этой реакции реагенты и ион металла взаимодействуют с ферментом независимо друг от друга, и ни один из компонентов реакции практически не влияет на прочность связи фермента с остальными компонентами. Вероятно, ион металла в данном случае выполняет роль активатора фермента и, возможно, фосфокреатина, облегчая его взаимодействие с нуклеофильным реагентом АДФ. [9]
Адсорбционный механизм регуляции активности гексокиназы скелетной мышцы ( II изозим гексокиназы) реализуется в повышении каталитической эффективности фермента вследствие нековалентной иммобилизации на митохондриальных мембранах. Связанная форма фермента по сравнению со свободной обладает большим числом оборотов, повышенным сродством к субстрату глюкозе и менее чувствительна к ингибирующему действию продукта реакции глюкозо-6 - фосфата. Связь фермента с наружной митохондриальной мембраной осуществляется преимущественно с участием фосфолипидного компонента мембран и регулируется внутриклеточными метаболитами. [10]
Альдолаза содержит свободные SH-группы; некоторые из них играют важную роль в каталитической активности, но основная их функция состоит в поддержании нативной структуры. В состав активного центра входят две е-аминогруппы остатков лизина. Их функция заключается в осуществлении связи фермента с одним из субстратов ( диоксиацетонфосфатом) путем образования промежуточного соединения типа основания Шиффа. [11]
Из всего сказанного выше ясно, что любая ткань животного или растительного организма может служить материалом для получения ферментов. Однако содержание ферментов в различных тканях далеко не одинаково; практически для извлечения ферментов удобнее использовать лишь те ткани и органы, которые богаты данным ферментом. Особенно важное значение при выборе подходящего объекта для получения ферментов имеют данные, характеризующие прочность связи фермента со структурными элементами клетки. Чем прочнее связан фермент с тканью, тем труднее использовать эту ткань как материал для получения ферментов. [12]
Из всего сказанного выше ясно, что любая ткань животного или растительного организма может служить материалом для получения ферментов. Однако содержание ферментов в различных тканях далеко не одинаково; нрактически для извлечения ферментов удобнее использовать лишь те ткани и органы, которые богаты данным ферментом. Особенно важное значение при выборе подходящего объекта для получения ферментов имеют данные, характеризующие прочность связи фермента со структурными элементами клетки. Чем прочнее связан фермент с тканью, тем труднее использовать эту ткань как материал для получения ферментов. [13]
Тиализильная пептидная связь, получающаяся в результате восстановления дисульфидных связей и S-аминоэтилирования образовавшегося остатка цистеина, также расщепляется трипсином ( см разд. Природа R имеет второстепенное значение, хотя связи Arg-Pro и Lys-Pro не разрываются. Известны и многие другие протеиназы, которые по своей специфичности напоминают трипсин. Например, известно, что тромбин разрывает участки Arg-Gly и Arg-Ser в фибриногене - одном из своих природных субстратов, однако для эффективного катализа необходима еще и связь фермента со вторым участком молекулы субстрата. Поэтому тромбин находит лишь ограниченное применение при расщеплении пептидных связей с целью изучения последовательности, хотя в случае секретина он разрывает связь Arg-Asp, в то время как три связи Arg-Leu остаются незатронутыми. Действие трипсина можно ограничить так, чтобы он разрывал либо по остаткам аргинина, либо по остаткам лизина. [14]
Микроэлементы также имеют важное значение для размножения и жизнедеятельности дрожжей, входя в состав ферментов, витаминов и других соединений, участвующих в их синтезе. Они влияют на скорость и характер различных биохимических процессов. Например, кобальт стимулирует размножение дрожжей, повышает содержание в клетках азотистых веществ небелковой природы, прежде всего ДНК, РНК и свободных аминокислот. Он стимулирует также синтез витаминов - рибофлавина и аскорбиновой кислоты. Стимулирующее действие микроэлементов объясняется тем, что они образуют с ферментами металлорганнче-ские и внутрикомплексные соединения. Получаемый эффект зависит от прочности связи фермента с молекулой субстрата или активации субстрата в промежуточном активном комплексе. [15]
Страницы: 1