Связь - группа
Cтраница 4
Утрата возможности свободного вращения вокруг линии связи азот - углерод приводит к появлению цис-транс-изомерии, причем транс-изомеры более стабильны и именно они и встречаются в большинстве белков. Так как вращение вокруг связей группы ( СО-NH) - атомы углерода возможно, то конфигурация белковых молекул должна представлять собой цепочку, в которой чередуются плоские элементы ( СО-NH) и гибкие звенья. Фактически структура упрочняется частично за счет водородных связей азота и кислорода и приобретает вид спирали. [46]
Группировка показателей заключается в следующем. Рассчитывают и заполняют матрицу связи групп исходных показателей задач. Определяют коэффициент связи новой группы со всеми другими группами и объединяют с группой Р группу показателей, у которой коэффициент связи с ней максимален. [47]
Спектральные данные выявили много новых примеров соединений, в которых группы XCN связаны с атомами переходных металлов обоими концами. Все три соединения молекулярные, причем в первых двух связь группы SCN с Hg осуществляется через серу, а в Zn ( NCS) 2 - через азот. В отношении соединений ртути этот результат не слишком неожидан, если принять во внимание молекулярное строение кристаллов HgCl2 и многих ртутьорганических соединений RHgX, где R - органический лиганд, Х С1, Br, J, SCN. Интересно, однако, нарушение аналогии в поведении родано - и селеноцианатных групп: Hg ( SeCN) 2, судя по частоте v ( CN), имеет мостиковую структуру. С другой стороны, весьма неожиданна молекулярная структура Zn ( NCS) 2, поскольку Zn в отличие от Hg обычно предпочитает координационные структуры ( с координационным числом 4 или 6) даже в простых соединениях. [48]
Схему ( 1, 1) можно упрощенно изобразить различными способами: мы можем опустить кружки и при А, В, С, D оставить только точки; иногда реагирующие атомы мы заключаем в рамку. Самый сжатый способ - это указание только атомов и связей индексной группы, расположенных так, что при реакции разрываются две вертикальные связи и возникают две горизонтальные. Тогда вся схема ( 1, 1) целиком передается индексом. [49]
Разница между ионами внешней и внутренней сфер существенна. Если ионы внешней сферы удерживаются за счет сил электростатического притяжения, то связь групп внутренней сферы с центральным атомом в случае неравновесных комплексов ( а иногда и равновесных) приближается по своему характеру к ковалентной. Из раствора при этом можно выделить тетрамминплатина ( II) нитрат. С другой стороны осадок AgCl при добавлении AgNO3 к раствору транс-изомера [ Pt ( NH3) 2Cl2 ] появляется лишь спустя некоторое время и в незначительном количестве. Причины появления осадка AgCl обусловлены взаимным влиянием атомов в молекуле; стр. [50]
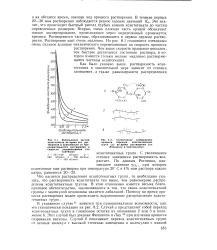 |
Измельчение частиц ксантогената во время его растворения в зависимости от продолжительности растворения и скорости перемешивания ( по.| Схематичное изображение. [51] |
Что касается распределения ксантогенатных групп, то необходимо указать, что растворимость ксантогената тем выше, чем равномернее распределены ксантогенатные группы. В этом отношении имеется весьма благоприятное обстоятельство, заключающееся в том, что связь ксантогенатной группы с молекулой целлюлозы является лабильной. Поэтому во время процесса растворения может происходить выравнивание распределения ксантогенатных групп. [52]
Из табл. 30 видно, что чем больше транс-влияние противолежащего лиганда, тем больше уменьшение частоты, отвечающей связи Pt-H. Авторы работы считают, что эти данные согласуются с представлением о том, что транс-активные лиганды ослабляют связь группы, расположенной в транс-положении к ним. Наряду с этим они не считают, что такое ослабление связи является основной причиной протекания реакций замещения в транс-положении к активному лиганду ( стр. [53]
Страницы: 1 2 3 4