Связь - гидроксильная группа
Cтраница 1
Связь гидроксильных групп или кислорода с кремнием имеет, скорее, более ковалентный, чем ионный характер. При кажущемся на первый взгляд простом определении количества силанольных групп на поверхности силикагеля возникают неожиданные противоречия. Для сильно гидратированных поверхностей число силанольных групп, определенное большинством химических реакций, никогда не достигает расчетных величин, в то время како число активных атомов водорода, вычисленное для площади 100 А, превышает пять. [1]
 |
Схематическое соотноше. [2] |
В системах, содержащих водные растворы щелочей, существенную роль играет характер связи гидроксильных групп. Гидро-ксильные группы могут быть связаны предпочтительно с атомами алюминия, а не кремния, как это имеет место в случае глинистых минералов, кристаллизующихся также при достаточно низких температурах. [3]
Природа гидроксильных групп на окиси алюминия была изучена Пери и Ханнаном [44] при помощи инфракрасной спектроскопии; они нашли, что связь гидроксильных групп с поверхностью носит преимущественно ионный характер. Гидроксильные группы легко обменивают водород, но скорость обмена значительно ниже, чем скорость изомеризации бутена-1 в бутен-2 на том же самом катализаторе. [4]
Как и при реакции с серной кислотой, возможность различать отдельные группы спиртов реакцией с хлоридом цинка основана на разной прочности связи гидроксильной группы. Реакции мешают многие другие компоненты смесей растворителей; в присутствии углеводородов эта реакция совсем не пригодна. [5]
Однако если принять во внимание только энергии ковалентных связей, то величины энергий связи расположатся в обратном порядке3, так как не менее 40 % энергии связи гидроксильной группы обусловлено частично ионным характером. Действительно, изучение химических реакций приводит к выводу, что часто группы ОН легче реагируют с нейтральными свободными радикалами, чем группы СН. Только таким путем можно удовлетворительно объяснить разрыв связи С-С гликоля при действии тетр а ацетата, свинца ( стр. [6]
Эта особенность в оптическом проявлении водородной связи, по мнению М. И. Батуева, объясняется большей ограниченностью в этих случаях пределов флюктуации в значениях межатомных расстояний и энергий связей гидроксильных групп. На более широком материале 6 ] им было показано, что основным признаком образования водородной связи вообще является не размытие частоты СН в полосу, как это считалось ранее, а смещение ее в сторону низких частот, которое в одних случаях сопровождается, а в других не сопровождается размытием линии в полосу. [7]
Если такую криптоконденсационную структуру привести в контакт с жидкой водой, она довольно быстро набухает, причем водородные связи, скрепляющие напряженные элементы структуры, распадаются и заменяются связями гидроксильных групп полимера с молекулами воды. Под действием внутренних напряжений в этих условиях пористая конденсационная структура вновь восстанавливается в том виде, какой она имела до высушивания. Восстановление структуры при увлажнении и сшивание ее при высушивании могут повторяться неограниченное число раз. [8]
К тому же степень диссоциации в ряду гидроокисей Ве ( ОН) 2, Mg ( OH) 2, Ca ( OH) 2, Sr ( OH) 2 и Ва ( ОН) 2 возрастает слева направо в связи с увеличением радиусов катионов и тем самым уменьшением их ионных потенциалов в том же направлении, что приводит к уменьшению связи гидроксильных групп с последними. [9]
Поскольку азот более электроотрицательный элемент, чем углерод, то связующее электронное облако смещено к азоту, в результате электронная плотность на азоте возрастает и он прочнее удерживает ион водорода. В этом случае связь гидроксильной группы ослабевает, она делается более подвижной, что приводит к усилению основных свойств аминов по сравнению с аммиаком. [10]
Рассматривая направление перегруппировки несилш-диметилди-фенилэтиленгликоля, можно вывести заключение, что большей способностью к отщеплению обладает та гидроксильная группа, которая находится у углеродного атома, связанного с фенилами. Тиффено объяснил такую неравноценность связи гидроксильных групп, исходя из представлений Вернера о переменной валентности, и ввел понятие о сродспгвоемкосгтш радикалов. Он считал, что чем больше сродствоемкость радикала, тем больше сродства на связь с ним затрачивает соединенный с этим радикалом углеродный атом и тем меньше у этого атома остается сродства на связь с гидроксилом. Путем изучения пинаколиновых перегруппировок многих несимметричных пи-наконов, содержащих попарно сравниваемые группы, были составлены ряды радикалов, расположенных в порядке убывания сродст-воемкости; эти ряды использовали в течение двух десятилетий при разрешении различных теоретических проблем. [11]
Рассматривая направление перегруппировки несыл-диметилди фениленгликоля, можно вывести заключение, что большей спосоС ностью к отщеплению обладает та гидроксильная группа, котора находится у углеродного атома, связанного с фенилами. Тиффен объяснил такую неравноценность связи гидроксильных групп, ис ходя из представлений Вернера о переменной валентности, и вве. Он считал, что чем больш сродствоемкость радикала, тем больше сродства на связь с ним за трачивает соединенный С этим радикалом углеродный атом и те. Путем изучения пинаколиновых перегруппировок многих несиммет ричных пинаконов, содержащих попарно сравниваемые группы, быт составлены ряды радикалов, расположенных в порядке убываню сродствоемкости; эти ряды использовали в течение двух десяти лети i при разрешении различных теоретических проблем. В настоящее вре мя имеются более четкие представления электронной теории. Согласно этим представлениям преимущественное течение процесса при пинаколиновой перегруппировке только в одном направлении обусловливается различной склонностью к диссоциации по связи QQ; изомерных оксониевых соединений ( стр. [12]
Суммируя, следует сказать, что химия поверхности ТЮ2 во многих отношениях напоминает поверхностные свойства силикагеля. В обычных условиях поверхность покрыта гидроксильными группами. Отражая характер связи внутри кристалла ТЮ2, связь гидроксильной группы с поверхностью является более ионной. [13]
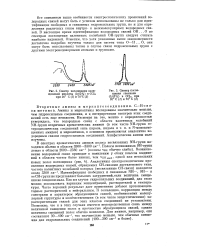 |
Спектр поглощения салициловой кислоты ( 0 05 % в СС14 при 20 С ( 1 и 70 С ( 2.| Спектр поглощения гваякола ( 0 01 % в СС14 при 20 С ( 1 и 70 С ( 2. [14] |
Все описанные выше особенности спектроскопических проявлений водородных связей могут быть с успехом использованы не только для идентификации свободных и связанных гидроксильных групп, но и для определения различных типов внутри - и межмолекулярных водородных связей. О по спектрам поглощения валентных колебаний ОН-групп следует считать наиболее надежной. О, они могут быть использованы также в случае связи гидроксильных групп с другими электронодонорными атомами и группами. [15]
Страницы: 1