Донорно-акцептор-ная связь
Cтраница 2
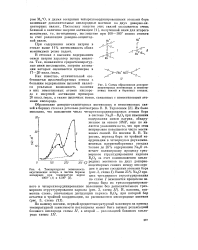 |
Схемы образования донорно-акцепторных мостиковых и немостиковых связей в боратных стеклах. [16] |
Поскольку энергия этих связей оказывается очень близкой к величине энергии активации [1 ], полученной нами для второго максимума, то, по-видимому, поглощение при 160 - 180 можно отнести за счет релаксации донорно-акцептор-ной связи. [17]
Обычно же циклоалкильные группы ведут себя как более энергичные доноры электронов, как показывают, например, значения о [26], а также результаты опытов Е. Н. Гурьяновой и И. Г. Арзамановой [27] по определению теплот образования - ДЯ) комплексов иода с сульфидами и дипольных моментов ( Д [) межмолекулярной донорно-акцептор-ной связи в комплексах, которая осуществляется с участием свободной электронной пары атома серы. [18]
При этом уменьшается потенциальная энергия системы и выделяется эквивалентное количество энергии. Донорно-акцептор-ная связь является разновидностью ковалентной связи. [19]
Таким образом, представление об электронных донорно-акцеп-торных связях позволяет исследовать связи в комплексе тригало-генида бора с аммиаком, кристаллическом ВеС12, гидратированных катионах и аммиачных комплексах с водой, окислах хлора и даже в окиси ксенона. Мы видим, что электронную донорно-акцептор-ную связь можно встретить в молекулах самых различных типов. Еще более важно то, что эта связь снова демонстрирует уже известное нам правило: образование любой связи происходит потому, что электроны оказываются одновременно вблизи двух ядер. Наличие незаполненной валентной орбитали позволяет участвовать в связи в ничуть не меньшей степени, чем если бы валентная орбиталь атома была заполнена наполовину. Атом ( или молекула), у которого имеется пустая валентная орбиталь, должен найти партнера, которому нужно избавиться от своих валентных электронов, - донора электронов. Атому ( или молекуле), валентная орбиталь которого заполнена лишь наполовину, необходимо найти партнера с такой же заселенностью орбиталей - другой атом с наполовину заполненной валентной орбиталью. Атом или молекула продолжает проявлять остаточную способность к образованию связи до тех пор, пока не использует с максимальной эффективностью все валентные орбитали. По существу это просто перефразированное классическое правило: атом стремится достичь конфигурации инертного газа. [20]
Согласно электронной теории основание - это вещество, поставляющее электронные пары для образования химической связи - донор электронных пар; кислота - вещество, принимающее электронные пары, - акцептор электронных пар. Кислотно-основное взаимодействие, согласно электронной теории, заключается в образовании донорно-акцептор-ной связи. В результате взаимодействия кислоты с основанием образуется солеподобный продукт, который называют аддиционным соединением, или аддуктом. Обычно аддукты удается выделить как индивидуальные вещества. [21]
Если первичная сольватная оболочка образуется за счет специфической сольватации, вопрос о числе молекул растворителя, непосредственно окружающих ион, становится более определенным. Поскольку в этом случае образование первичного сольватного комплекса осуществляется вследствие слабых донорно-акцептор-ных связей, число молекул растворителя, способных выступать в качестве лигандов по отношению к данному иону, определяется типом гибридизации молекулярных орбиталей последнего. [22]
 |
Прибор для диэлектрометрического титрования. [23] |
На основе определения диэлектрической проницаемости растворов был разработан метод физико-химического анализа, который дает возможность определять состав и относительную устойчивость образующихся комплексов. Однако предложенная Шека методика не позволяет непосредственно определять одну из важнейших констант соединений с донорно-акцептор-ными связями - их дипольные моменты. Обычно для определения последних комплексы специально синтезируют, выделяют и далее измерения проводят по общепринятой методике в растворах. Если учесть, что при этом применяются разбавленные растворы, где возможна диссоциация комплексов на компоненты, то станет ясным, что получение надежных результатов в этих условиях затруднительно. [24]
Раствор аммиака в воде обладает слабыми щелочными ( основными) свойствами. Причина основных свойств аммиака - наличие у атома азота неподеленной электронной пары, которая участвует в образовании донорно-акцептор-ной связи с ионом водорода. По этой же причине амины также являются слабыми основаниями. [25]
Водородная связь возникает в результате междипольного взаимодействия двух сильно полярных связей, принадлежащих различным молекулам ( или одной и той же молекуле), но она в значительной степени усиливается вследствие взаимной поляризации связей, обусловленной указанными особенностями водородного атома. С другой стороны, деформация молекул, вызываемая образованием водородной связи, в соответствующих случаях способствует образованию донорно-акцептор-ных связей. [26]
Сульфиды взаимодействуют также с кислотами Льюиса. Методом криоскопии найдено [92], что диалкилсульфиды, а также тио-фан и его производные образуют с бромистым алюминием комплексы состава 1: 1, причем теплота образования донорно-акцептор-ной связи как с ароматическими, так и с алифатическими сульфидами, одна и та же. [27]
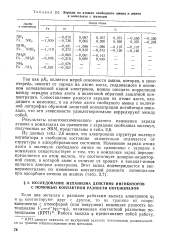 |
Заряды на атомах свободного амина и амина в комплексе с железом. [28] |
Из данных табл. 2 6 видно, что электронная структура молекул ингибитора в свободном состоянии значительно отличается от структуры в адсорбированном состоянии. Изменение заряда атома азота в молекуле свободного амина по сравнению с зарядом в комплексе свидетельствует о том, что в комплексе заряд перераспределяется на атом железа, что соответствует донорно-акцептор-ной связи, в которой амин в отличие от хромат - и ванадат-ионов является донором электронов. [29]
При образовании этих соединений приближение к комплексообразователю отрицательно заряженных ионов сопровождается возникновением сил отталкивания. Поэтому для возникновения донорно-акцептор-ных связей необходима высокая интенсивность поля центрального иона, что достигается при его малом радиусе и большом заряде. Если комплексообразователь представляет собой катион очень малого радиуса, то между самими лигандами - противоионами возникают столь значительные силы отталкивания, что их сближение и тем более соприкосновение с комплексообразователем становится невозможным. Таким образом, для ионов-комплексообразователей очень малого радиуса образование ацидокомплексов с большим числом лигандов маловероятно. Наиболее благоприятные для комплексообразования характеристики имеют атомы d - и / - элементов. Их предвнешний или третий снаружи электронный слой содержит незаполненные подуровни и характеризуется значительной подвижностью орбиталей. Поэтому ионы таких элементов склонны к образованию комплексных соединений с лигандами - донорами электронных пар. В образующихся связях участвуют d - и / - орбитали. [30]
Страницы: 1 2 3