Ко-валентная связь
Cтраница 2
Что называется обменным механизмом образования ко-валентной связи. [16]
Такая двухэлектронная двухцентровая связь называется ко-валентной связью. [17]
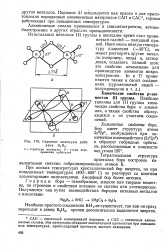 |
Строение молекулы дибо-рана В2Нв. [18] |
Тетрагональная структура кристалла бора построена ко-валентными связями гибридизированных атомов В. [19]
В предыдущей главе были рассмотрены типы ко-валентных связей и их физические свойства. Вопрос о том, какие изменения претерпевают электронные облака связей в молекуле при смене заместителей или при введении вместо водорода заместителя, совершенно не затрагивался. Также не рассматривался вопрос о влиянии заместителей друг на друга. [20]
Первичную структуру белковой молекулы составляет скелет ко-валентных связей, в том числе ковалентные мостиковые связи, подобные дисульфидной или фосфатной. [21]
МО приписывает расщепление в основном образованию ко-валентной связи. [22]
Однако существует и другой механизм образования ко-валентной связи, который называется донорно-акцептор-ным механизмом. Ковалентная связь, которая образуется по донорно-акцепторному механизму, назьтается донорно-ак-цепторной связью. [23]
Первичную структуру белковой молекулы составляет скелет ко-валентных связей, в том числе ковалентные мостиковые связи, подобные дисульфидной или фосфатной. [24]
Чем объясняется пространственная направленность и насыщаемость ко-валентных связей. [25]
С повышением температуры возрастает число разрывов ко-валентных связей и увеличивается количество свободных электронов в кристаллах чистых полупроводников. [26]
Участие d - орбиталей в образовании поверхностной ко-валентной связи приводит к представлению, что чем больше процент d - характера, как его определяет Полинг, тем меньшее число орбиталей оказывается доступным для образования поверхностной связи с веществами, подобными водороду. На кислород, легко принимающий электроны из s - или р-зоны, эта характеристика металлов не влияет. [27]
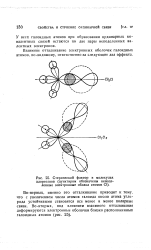 |
Стерический фактор в молекулах хлорэтанов ( пунктиром обозначены неподеленные электронные облака атомов С1. [28] |
У всех галоидных атомов при образовании ординарных ко-валентных связей остаются по две пары неподеленных валентных электронов. [29]
В решетке алмаза оно определяется числом ко-валентных связей атомов С с соседними. Алмазный тип решетки имеют важнейшие элементные полупроводники - кремний, германий, а также и а-олово. [30]
Страницы: 1 2 3 4