Слабейшая связь
Cтраница 2
Разветвление цепи произойдет, если энергии возбуждения R02 будет достаточно либо для образования из него бирадикала и нового радикала ( при мономолекулярном распаде), либо, при бимолекулярном взаимодействии, для дальнейшего распада по слабейшей связи образующейся молекулы. [16]
Разветвление цепи произойдет, если энергии возбуждения RC2 будет достаточно либо для образования из него бирадикала и нового радикала ( при мономолекулярном распаде), либо, при бимолекулярном взаимодействии, для дальнейшего распада по слабейшей связи образующейся молекулы. [17]
В случае гексана и более длинных нормальных парафинов распад приводит к образованию больших количеств а-олефинов, содержащих слабую связь С-С, сопряженную с двойной. Слабейшая связь С-С в середине углеродной цепи имеет прочность 318 кДж / моль ( 76 ккал / моль) в н-гексане, 314 кДж / моль ( 75 ккал / моль) в н-гептане и 310 кДж / моль ( 74 ккал / моль) в м-октане и в более длинных. [18]
При описании свойств таких токсинов, как агрегатов нескольких доменов, обычно используется понятие четвертичной структуры. Хотя гидрофобные силы сцепления относятся к слабейшим связям, в сумме они благодаря многочисленности дают значительную энергию взаимодействия. [19]
С - Н связей такого ж-е типа, как и молекулы асфальтенов, тепловой эффект равен нулю. В хорошем растворителе асфальтенов всегда имеются алкилароматические углеводороды, у которых слабейшими связями С - Н являются связи ArCH ( R) - Н, несколько менее прочные, чем связь ArCHs - Н, в результате влияния R. Таким образом, реакция гибели асфальтенового радикала при взаимодействии с молекулой растворителя в действительности должна быть. По правилу Поляли - Семенова энергия активации таких реакций равна - Пккал / моль. [20]
Они отметили, что распад возбужденных молекул RF может происходить не только с разрывом слабейших связей, но и по бирадикалытому механизму. [21]
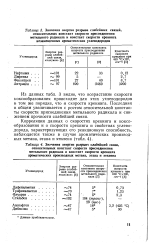 |
Значения энергии разрыва слабейших связей.| Значения энергии разрыва слабейшей связи. [22] |
Из данных, табл. 3 видно, что возрастание скорости коксообразования происходит для этих углеводородов в том же порядке, что и скорости крекинга. Последняя в общем увеличивается с ростом относительной константы скорости присоединения метильного радикала и снижением прочности слабейшей связи. [23]
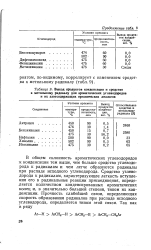 |
Выход продуктов конденсации и сродство. [24] |
В общем склонность ароматических углеводородов: к конденсации тем выше, чем больше сродство углеводорода к радикалам и чем легче образуются радикалы при распаде исходного углеводорода. Сродство углеводорода к радикалам, характеризующее легкость вступления его в радикальные реакции присоединения, определяется количеством конденсированных ароматических колец и, в значительно большей степени, типом их конденсации. Прочность слабейшей связи, определяющая скорость образования радикалов при распаде исходного углеводорода, определяется типом этой связи. [25]
Образование кокса при термическом разложении ароматических углеводородов происходит, в зависимости от их строения, с различной скоростью. Так, скорость коксообразования убывает в ряду: нафтацен а-метилантрацен р-метилантрацен антрацен 1 6-диметилнафталин нафталин. Склонность ароматических углеводородов к образованию кокса возрастает со снижением прочности слабейшей связи в их молекуле и повышением скорости их вступления в реакцию присоединения с радикалом. Способность углеводорода вступать в эту реакцию можно охарактеризовать так называемым сродством к метильному радикалу, которое измеряется отношением констант скорости присоединения метильного радикала к молекуле данного углеводорода и углеводорода, принятого за эталон. [26]
При нагреве гидроперекиси бурно распадаются по механизму свободных радикалов или, в присутствии кислоты, - по ионному механизму. В каждом случае образуются специфичные карбонильные и гидроксильные соединения. Третичные алкильные гидроперекиси разлагаются по связи О-О, за которой следует разрыв слабейшей связи С-С. Вторичные алкильные гидроперекиси образуют кетоны, а первичные. [27]
Адиабаты Гюгонио кетонов, кислот, сложных эфиров и амидов, в структуре молекул которых есть связь С О, имеют особенности при массовых скоростях UP около 2.5 мм / мкс и 7 1.1 - 1.4 К. Эти температуры примерно в 1.5 - 2 раза меньше тех, которые ожидались из кинетических данных для мономолекулярного распада паров соединений указанных классов. Похоже, что превращения за фронтом ударной волны всех соединений с кратной связью в структуре молекулы идут на начальной стадии не через разрыв слабейшей связи, а образование промежуточного продукта, который отсутствует в исследованиях с парами. [28]
Замена водорода в нафталиновых кольцах на метальные группы резко повышает скорость коисообразования. При этом наличие метильной группы в а-положении оказывает значительно большее влияние, чем в других, даже при меньшем числе метальных групп: скорость новообразования при разложении а-метилнафталина меньше, чем 1 6-диметилнафталина, но больше, чем в случае 2 6-диметилнафталина. В табл. 2 для производных нафталина, расположенных в порядке возрастания скорости коисообразования при их крекинге, приведены значения констант скорости крекинга и энергии разрыва слабейших связей в их молекулах. [29]
В случае сложных многоатомных молекул не представляется возможным проведение подобного рода расчетов энергетических состояний. Все известные до сих пор спектры индивидуальных соединений получены опытным путем. Достаточно строгий теоретический расчет распределения интен-сивиостей в масс-спектре удалось произвести только для молекулы Нг - Масс-спектры многоатомных молекул слишком сложны, чтобы их можно было рассчитать, исходя из простейших представлений, о выбивании из молекулы ионизирующим электроном валентного электрона с распадом образовавшегося иона по слабейшим связям. [30]
Страницы: 1 2 3