Довольно слабая связь
Cтраница 1
Довольно слабая связь между двумя атомами, осуществляемая с участием атома водорода и известная под названием водородной связи, может играть важную, а иногда и определяющую роль в стереохимии молекул. Неустойчивость этой связи, в особенности при термическом возбуждении и действии растворителей, приводит к тому, что ее влияние на стереохимию молекул оказывается наиболее эффективным в твердых телах ( кристаллах, макромолекулах, волокнах) и соответственно все менее эффективным в жидкостях, растворах и парах. [1]
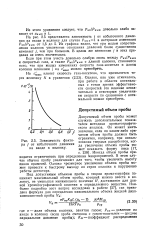 |
Зависимость факто - зовании Твердь1х адсорбентов, ког. [2] |
Если при этом учесть довольно слабую связь между Рщ / Рвых и скоростью газа, а также Рвх / выт с длиной колонки, становится ясно, что при малых изменениях скорости газа-носителя и длины колонки влиянием j на с акс можно пренебречь. [3]
Продуктом реакций присоединения являются соединения, образующиеся с помощью довольно слабых связей между целлюлозой и реагирующей ере-дои, например с помощью водородных мостиков или притяжения к полярным группам вдоль молекулы целлюлозы. Именно в результате таких реакций образуются щелочная, аммиачная и аминовая целлюлозы, продукты присоединения к неорганическим кислотам, четвертичным аммониевым основаниям и др. Эти соединения являются довольно нестойкими и могут легко гидроли-зоваться водой, образуя целлюлозу обычно в гидратной форме. [4]
При фотолизе 1 2-дииодбензола ( 72) для образования дегидробензола необходимо расщепить только довольно слабую связь иод-углерод. [5]
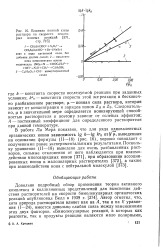 |
Влияние ионной силы. [6] |
Автор отметил, что, хотя природа растворителя влияет как на Л, так и на Е уравнения ( I-24), имеется довольно слабая связь между изменениями этих двух факторов. [7]
Молекулярные кристаллические решетки образуются из полярных молекул, между которыми возникают силы взаимодействия, так называемые ван-дер-ваальсовы силы, имеющие электрическую природу. В молекулярной решетке они осуществляют довольно слабую связь. Молекулярную кристаллическую решетку имеют лед, природная сера и многие органические соединения. [8]
Для всех случаев химической связи имеется обратное соотношение между прочностью связи и ее межатомным расстоянием. Водородные связи вообще, будучи довольно слабыми связями, имеют большее межатомное расстояние, чем ковалентные связи. [9]
Отличительной чертой элементов, расположенных в последней группе периодической системы, является. Известно только несколько соединений ксенона с довольно слабыми связями и только одно соединение криптона - для аргона, неона или гелия пока не получено ни одного соединения. Общее название этих элементов - инертные газы - хорошо отражает их свойства. Причина их инертности понятна с точки зрения традиционных правил связи и заселенности орбиталей. Все валентные орбитали заполнены, так что у атомов не остается возможности для образования нормальных химических связей. [10]
Это бесцветное твердое вещество при комнатной температуре легко сублимируется с образованием крупных прозрачных кристаллов. В этом соединении сохраняются группировки XeFz и XeF4, которые удерживаются, по-видимому, довольно слабой связью. [11]
Вода, содержащаяся в перлите в количестве немного более 1 2 %, удерживается очень слабо и поэтому легко удаляется. По мере дегидратации остающаяся вода удерживается все более прочно, и именно эта вода обусловливает расширение стекловатых пород при нагревании. Существует теория, согласно которой вода перлитовых стекол не связана в форме гидроксильных групп. Кажущаяся теплоемкость абсорбированной воды говорит в пользу довольно слабой связи, поскольку она превышает теплоемкость льда при температуре выше 75 С, а также при комнатной температуре. [12]
Страницы: 1