Термодинамическая связь
Cтраница 1
Термодинамическая связь 250 Томсона постулат 115 ел. [1]
Термодинамическая связь процессов тепло - и массообмена. [2]
Существует термодинамическая связь между k lt kit XBH H TgH [48], соотношение - скоростей прямой и обратной катализируемой основаниями ионизации определяется константами диссоциации двух кислотных частиц. [3]
Существует термодинамическая связь между k lt kit КВК лК5н [ 8], соотношение скоростей прямой и обратной катализируемой основаниями ионизации определяется константами диссоциации двух кислотных частиц. [4]
Но одно установление указанной термодинамической связи недостаточно. Это объясняется тем, что систему ( законы сохранения массы и энергии, уравнения баланса энтропии и состояния) еще нельзя решить, так как в ней содержатся в качестве неизвестных переменных необратимые потоки, в то время как в качестве начальных и граничных условий при расчетах задаются параметрами состояния ( давлением, температурой, концентрацией) или их производными. [5]
Это уравнение характеризует термодинамическую связь поля перемещений и поля температур. [6]
Между обоими эффектами имеется простая термодинамическая связь. [7]
Для иллюстрации способа установления термодинамических связей и функций при помощи перечисленных параметров вычислим некоторые из них. [8]
При изображении поверхностей ПЭ не будет сделано никаких попыток изобразить термодинамическую связь между реагентами и продуктами реакции. В настоящий момент это невозможно осуществить в какой-либо простой качественной форме. Скорее, мы изобразим энергию реакционной системы, начиная с некоторого большого межмолекулярного расстояния и кончая некоторым небольшим межмолекулярным расстоянием, которое все еще превышает межмолекулярное расстояние в продукте. В результате влияние термодинамики на скорости реакций следует рассматривать независимо от нашего подхода. [9]
В том случае, когда газовая фаза при давлении и температуре, соответствующих критической точке расслаивания, с приемлемой степенью приближения может быть принята за смесь идеальных газов, экспериментальное исследование может несколько упроститься. В силу известной термодинамической связи химического потенциала с парциальным давлением компонента вместо изучения зависимости р - V - Т - N достаточно ис - следовать зависимость парциального давления компонентов от состава раствора в критической области. [10]
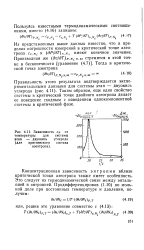 |
Зависимость СР от температуры для системы эган - двуокись углерода ( для критического состава азеотропа. [11] |
Концентрационная зависимость энтропии вблизи критической точки азеотропа также имеет особенность. Это следует из термодинамической связи между энтальпией и энтропией. [12]
Разумеется, всякое необратимое явление, независимо от его вида и происхождения, сопровождается возрастанием энтропии изолированной системы взаимодействующих тел. Однако причины возникновения и связанные с ними особенности проявления необратимости определенного вида сказываются на структуре термодинамических связей, описывающих ход изменения состояний системы. Иными словами - характер соотношений между термодинамическими параметрами в необратимом процессе зависит от природы явлений, вызывающих необратимые изменения. [13]
Существенно новая и дискуссионная точка зрения высказывается в отношении явлений обрыва и особенно инициирования цепных реакций стенками сосуда. Излагается теория возникновения свободных радикалов на поверхности твердых тел, особенно полупроводников. Устанавливается термодинамическая связь между обрывом и генерированием свободных радикалов цепи стенкой. Выясняются двойственная роль стенки и условия, в которых последняя выступает как замедлитель или ускоритель цепной реакции. Показана инициирующая роль стенки как результат более легкого зарождения радикалов на ней, чем зарождение радикалов в объеме. Разбираются вопросы гетерогенного инициирования радикалов в присутствии примесей. [14]
Если исходить из таких физических предпосылок и принять, что пограничная кривая вблизи критической точки является аналитической кривой, можно получить новые термодинамические уравнения, связывающие значения скачков производных некоторых свойств ( как для чистых веществ, так и для растворов) с формой пограничной кривой вблизи критической точки. При этом было показано, что в случае, когда пограничная кривая является параболой второй степени, скачок этих производных при пересечении пограничной кривой в критической точке имеет конечное значение. Если же кривая имела бы вблизи критической точки плоский участок или была бы кривой более высокого порядка, чем второй, скачки имели бы бесконечно большое значение. Таким образом, центральный вопрос теории критических явлений может получить однозначный ответ, если только установить экспериментально, конечное или бесконечное значение имеет скачок, скажем, ( dv / dT) P: N или Ср для двойных растворов, или cv для чистых веществ. Термодинамическая связь между скачками производных различных величин ( например, ( dvldT) P: N и СР, ) Дает дополнительную возможность проверки как правильности экспериментального исследования различных скачков, так и правильности посылок, положенных в основу классической теории, и тех новых термодинамических соотношений, которые подвергаются проверке. Таким образом, появились новые и термодинамический, и экспериментальный методы исследования критических явлений. [15]
Страницы: 1