Сгорание - углерод
Cтраница 1
Сгорание углерода и водорода, связанных между собой в различные соединения ( углеводороды), протекает значительно сложнее, чем свободных углерода и водорода. Наличие, например, тройной связи в углеводородах ( ацетиленовые) повышает их теплоту сгорания. [1]
Сгорание углерода до ССЬ не ведет к увеличению количества молекул газов и не влияет на давление в трубке для сожжения. [2]
Сгорание углерода и водорода, связанных между собой в различные соединения ( углеводороды), протекает значительно сложнее, чем свободных углерода и водорода. Наличие, например, тройной связи в углеводородах ( ацетиленовые) значительно повышает их теплоту сгорания. [3]
Реакция сгорания углерода: С О2 СС; на 12 кг С требуется 32 кг О2, значит, удельный расход кислорода на 1 кг углерода составляет 32 / 12 2 67 кг О / кг С. [4]
Теплоты сгорания углерода и водорода значительно различаются. Наилучшим соотношением С и Н обладают парафиновые углеводороды, наихудшим - ароматические, особенно би - и трициклические углеводороды. [5]
Теплота сгорания углерода С равна 94 ккал / моль, а его мол. [6]
 |
Положение уровня 0 ядра вС12, играющего большую роль в эволюции. [7] |
Реакции сгорания углерода и кислорода и последующие реакции представляют большой интерес для теории происхождения элементов. Соответствующие им стадии эволюции мы рассмотрим в следующем параграфе. [8]
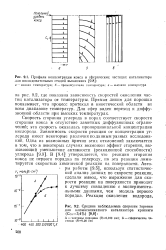 |
Профили концентрации кокса в сферических частицах катализатора для последовательных стадий выжигания.| Средние наблюдаемые скорости горения для алюмосиликатного катализатора крекинга ( ССо3 4 %. [9] |
Скорость сгорания углерода в порах соответствует скорости сгорания кокса в отсутствие заметных диффузионных ограничений; эта скорость оказалась пропорциональной концентрации кислорода. Зависимость скорости реакции от концентрации углерода имеет некоторые различия по данным разных исследований. В [9.4] утверждается, что реакция сгорания кокса не первого порядка по углероду, но эта реакция лимитируется скоростью химической реакции на поверхности. Авторы работы [9.5], используя статистический анализ данных по скорости реакции, сделали вывод, что выражение для скорости реакции на поверхности приводит к лучшему совпадению с экспериментальными данными, чем модель первого порядка. [10]
Процесс сгорания углерода [3] в слое составляется из двух зон ( стадий): кислородной ( в которой образуется как СО2, так и СО) и восстановительной. Процесс разложения углекислоты, начинающийся в кислородной зоне, переходит в чисто восстановительную зону. [11]
Теплота сгорания более сложных углеродов ( с двойными и тройными связями), а также многочисленных замещенных не может быть вычислена по формуле ( I. Караша электроны атомов углерода и водорода данных соединений несколько смещены по отношению к тому положению, какое они занимают в молекулах простых углеводородов. Поэтому и теплота сгорания несколько изменяется в большую или меньшую сторону. [12]
При сгорании углерода у фурм доменной печи в продуктах горения получается окись углерода и азот. Углекислоты не может быть, так как при температурах выше 950 она. Однако эта реакция происходит в течение определенного времени, поэтому на некотором расстоянии от глазка фурмы в горновых газах содержится углекислота. Точно так же не сразу исчезает из горновых газов свободный кислород. Поэтому у каждой фурмы существует область, в которой имеются свободный кислород и углекислота. Эта область называется окислительной зоной; наличие и размеры ее оказывают большое влияние на работу доменной печи. [13]
При сгорании углерода образуется большое количество окиси углерода и углекислого газа, значительная часть которых находится в ванне расплавленного металла. При быстром остывании чугуна гязы и неметаллические включения не успевают выйти наружу, пбоазуя в нем поры и загрязнения. [14]
При сгорании углерода, связанного с гидроксильной группой, перемещаются только Три электрона. [15]
Страницы: 1 2 3 4