Среднее значение - энергия - активация
Cтраница 1
Среднее значение энергии активации для термического крекинга составляет от 50 000 до 60 000 кал / моль. [1]
Среднее значение энергии активации 64 ккал / моль прекрасно согласуется с недавно полученными данными [53, 82] для особо чистых графитов и сравнимо с величиной 58 4 ккал / моль. Но сразу обращает внимание, что максимальные температуры, при которых работали авторы [53] и [82], 625 и 637, значительно ниже, чем в данных исследованиях. Следовательно, полученная средняя величина заметно превосходит ранее определенные. Это можно объяснить более высоким содержанием каталитически активных твердых примесей в графитах, исследованных до настоящего времени. [2]
Интересно отметить, что среднее значение энергии активации для двух рассматриваемых галоидэтанов, равное 3370 кал, почти в точности равно энергии активации диффузии. Таким образом, в процессе диффузии движение одной молекулы относительно другой требует свободной энергии, значение которой лежит между значениями свободной энергии активации вязкого течения каждого из этих веществ в отдельности. [3]
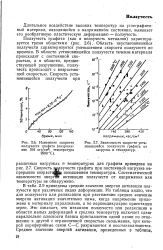 |
Изменение скорости ползучести графита ( напряжение 315 кгс / см2. температура 2500 С.| Зависимость скорости уста. [4] |
В табл. 2.9 приведены средние значения энергии активации ползучести при различных видах деформации. Из таблицы видно, что для ползучести или релаксации при растяжении среднее значение энергии активации значительно ниже, когда напряжение приложено к материалу параллельно, а не перпендикулярно ориентации зерен. Это означает, что механизм ползучести или релаксации в области малых деформаций и средних температур включает сдвиг параллельно плоскости базиса кристаллитов одной пачки по отношению к другой с ограниченной скоростью скольжения, при которой периферийные связи С-С разрываются и восстанавливаются. [5]
По некоторым данным, средние значения энергии активации некаталитических процессов составляют 30 - 45 ккал / моль, а для каталитических - 16 - 30 ккал / моль. [6]
По некоторым данным, средние значения энергии активации некаталитических процессов составляют 30 - 45 ккал / моль, я для каталитических - 16 - 30 ккал / моль. [7]
Из приведенных в табл. 5 данных получаем среднее значение энергии активации безбарьерного разряда при равновесном потенциале А0 22 9 1 ккал / молъ. [8]
При решении примера по варианту I сразу получаем среднее значение энергии активации. [9]
В 1939 г. Берк и Ласковский [26] определили среднее значение энергии активации при разложении парафиновых углеводородов С4 - С8; она равна 63 ккал / м оль. Тиличеев [27] приводит для нормальных парафиновых углеводородов С6 - С10 среднее значение энергии активации 65 ккал / моль, а для парафиновых углеводородов Си - С32 60 ккал / моль. Некоторые выводы основываются [28] на изучении термического разложения н-бутана в периодическом реакторе при начальном общем давлении 5 - 60 мм рт. ст. Константы скорости реакции первого порядка, уменьшающиеся с возрастанием степени превращения, экстраполировали к нулевой степени превращения. [10]
При решении примера по варианту I сразу получаем среднее значение энергии активации. [11]
Параметры активации процесса эпоксидирования определены во многих случаях. Среднее значение энергии активации обычно составляет 10 - 15 ккал / молъ. Однако обычно это значение довольно сильно изменяется в зависимости от строения олефина и гидроперекиси, а также типа катализатора. В табл. 19 приводятся литературные параметры активации для различных реакций. [12]
Бурк и Ласковский [ 14а ] обобщили данные по энергии активации разложения парафиновых углеводородов С - С8 и нашли, что средние значения ее для этих углеводородов лежат в пределах 63 000 500 кал. Тиличеевым приводится среднее значение энергии активации для нормальных Сй - С10 парафинов равное 65 000 кал и для Си - С32 равное 60000 кал. [13]
Кроме того, некоторые реакции могут протекать параллельно или последовательно с различными скоростями, накладываясь друг на друга. Во многих случаях можно говорить только о среднем значении энергии активации, которое имеет смысл только в ограниченном интервале температур. [14]
В 1939 г. Берк и Ласковский [26] определили среднее значение энергии активации при разложении парафиновых углеводородов С4 - С8; она равна 63 ккал / м оль. Тиличеев [27] приводит для нормальных парафиновых углеводородов С6 - С10 среднее значение энергии активации 65 ккал / моль, а для парафиновых углеводородов Си - С32 60 ккал / моль. Некоторые выводы основываются [28] на изучении термического разложения н-бутана в периодическом реакторе при начальном общем давлении 5 - 60 мм рт. ст. Константы скорости реакции первого порядка, уменьшающиеся с возрастанием степени превращения, экстраполировали к нулевой степени превращения. [15]
Страницы: 1 2