Высокое значение - потенциал - ионизация
Cтраница 2
С другой стороны, бор, находящийся слева от границы Цинтля и обладающий дефицитом электронов, в виде простого вещества характеризуется неметаллическими свойствами. Из-за кайносимметричности 2р - орбитали и вследствие этого высоких значений потенциала ионизации и электроотрицательности бора имеет место затруднение к обобществлению электронов в пределах всего кристалла. В силу дефицита валентных электронов в кристаллических модификациях бора наблюдается их обобществление, которое ограничено, однако, локальными атомными группами. Поэтому для бора характерны сложные кристаллические решетки, структурным элементом которых служит икосаэдр ( рис. 121), который является своеобразным кластером, состоящим из 12 атомов бора. [16]
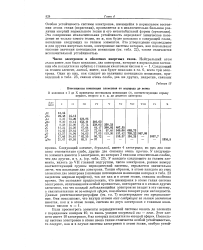 |
Потенциалы ионизации элементов от водорода до неона. [17] |
Эта совершенно исключительная устойчивость определяет химическое поведение не только самого гелия, но и, как будет показано в следующей главе, поведение следующих за гелием элементов. Это утверждение справедливо и для других инертных газов, электронные системы которых, как показывают высокие значения потенциалов ионизации ( см. табл. 22), также отличаются исключительной устойчивостью. [18]
Атомы некоторых элементов имеют такое электронное строение, что эти элементы оказываются довольно инертными в химическом отношении. Особенно инертна нулевая группа элементов периодической системы. Ее элементы характеризуются также высокими значениями потенциалов ионизации. Поэтому не удивительно, что элементы этой группы часто называют инертными газами, хотя лучше называть их благородными газами. Очевидно, электронное строение атомов этих элементов обладает особенной устойчивостью к изменениям. Другие атомы ( например, Na, F -, Ca2), изоэлектронные с атомами инертных газов, также довольно инертны в химическом отношении. [19]
Транспортируют и хранят гелий в газообразном состоянии в стальных баллонах при давлении р 15 МПа или в сжиженном состоянии при р 0 2 МПа. Стоимость гелия значительно выше, чем аргона, поэтому его применяют в основном при сварке химически чистых и активных материалов и сплавов, а также сплавов на основе алюминия и магния. Из-за способности обеспечивать повышение проплавления ( благодаря высокому значению потенциала ионизации) гелий применяют иногда в тех случаях, когда требуется получить большую глубину проплавления или специальную форму шва. [20]
Гелий - бесцветный, нетоксичный и невзрывоопасный газ, без запаха, значительно легче воздуха и аргона. Гелий для сварки поставляется по ТУ 51 - 689 - 75 трех марок: А ( с объемной долей чистого гелия 99 995 %), Б ( 99 99 %) и В ( 99 99 %) в стальных баллонах при давлении 15 МПа или в сжиженном состоянии при давлении до 0 2 МПа. В баллоне вместимостью 40 дм3, окрашенном в коричневый цвет, с белой надписью, содержится 6000 л газа. Гелий значительно дороже аргона, поэтому его применяют в особых случаях при сварке химически чистых и активных металлов и сплавов. Для сварки в гелии характерны большая глубина про-плавления ( благодаря высокому значению потенциала ионизации) и особая форма шва. [21]
Система, образуемая этими двумя электронами, отли - чается особой устойчивостью. Это следует прежде всего из чрезвычайно высокого значения потенциала ионизации гелия. Но еще отчетливее эта особая устойчивость системы электронов в нормальном атоме гелия проявляется при сравнении энергий, требующихся, с одной стороны, для перевода электрона с уровня Is на ближайший более высокий уровень 2s и, с другой стороны, для перехода электрона с уровня, например, 2s на уровень Зр ( ср. Первая равна 20 55 эв, а вторая - только 2 42 эв. Эта совершенно исключительная устойчивость определяет химическое поведение не только самого гелия, но и, как будет показано в следующей главе, поведение следующих за гелием элементов. Это утверждение справедливо и для других инертных газов, электронные системы которых, как показывают высокие значения потенциалов ионизации ( см. табл. 22), также отличаются, исключительной устойчивостью. [22]
Страницы: 1 2