Молекулярный сероводород
Cтраница 1
Молекулярный сероводород существует в кислотной среде ( рН 7), а при росте рН сероводород переходит в бисульфидное состояние; при дальнейшем увеличении рН ( 9 5) бисульфид превращается в растворимый сульфид и становится относительно безвредным. [1]
Ответственным за стимулирование процесса наводоро-живания металлов считается обычно [40,41,82,83] молекулярный сероводород. Элементарная сера или ее соединения, чтобы дать стимулирование наводороживанию, должна превратиться в гидрид и в таком виде адсорбироваться на поверхности металла. [2]
О - чН ( 110 2 ккал) [91], Участие растворенного молекулярного сероводорода в катодном процессе рассматривается рядом исследователей [41,60,69,129] в предположении, что скорость катодного процесса ограничивается при этом его диффузией. [3]
В нейтральных и щелочных средах содержится больше всего ионов гидросульфидов, в кислых средах - молекулярный сероводород, в сильнощелочных электролитах появляются в небольших количествах ионы сульфидов. [4]
В нейтральных и щелочных средах содержится больше ионов гидросульфидов, а в кислых средах - молекулярного сероводорода. [5]
Если предположить, что адсорбция происходит только за счет электростатического взаимодействия катионов ингибитора с отрицательно заряженной поверхностью металла через слой молекулярного сероводорода, то поскольку слой сероводорода может только ослабить это взаимодействие, эффективность защиты в этом случае должна была бы несколько снизиться, Следует допустить поэтому наличие специфической адсорбции катионов ингибитора на поверхностном слое сероводорода. Адсорбируясь на слое сероводорода, катионоактивный ингибитор создает энергетический барьер за счет ф - - потенциала, который препятствует подводу ионов гидроксония. Ингибитор таким образом блокирует молекулы сероводорода, уменьшая образование ионов сульфония. [6]
Было высказано предположение, что при совокупности ряда факторов в кислых растворах решающее значение имеет наво-дораживание, в области рН 4 - - 6 влияет адсорбция молекулярного сероводорода, а в более щелочных - защитное действие ионов гидроксила. [7]
В зависимости от величины рН среды равновесие реакций сдвигается вправо или влево: в нейтральных и щелочных средах содержится больше всего ионов гидросульфида, в кислых средах - молекулярный сероводород, в сильнощелочных электролитах появляются в небольших количествах ионы сульфида. В связи с хорошей растворимостью сероводорода в воде ( около 3000 мг / л при 30 С) происходит уменьшение величины рН водной фазы, вследствие чего основная часть сероводорода, абсорбируемая водной и углеводородной фазой, находится не в ионной, а в молекулярной форме. Fe H2S - FeS Н2 упрощенная и не отражает полностью механизм сероводородной коррозии. [8]
В зависимости от величины, рН среды равновесие реакций сдвигается вправо или влево: в нейтральных и щелочных средах содержится больше всего ионов гидросульфидов, в кислых средах - молекулярный сероводород, в сильнощелоч ных электролитах появляются ионы сульфидов в небольших количествах. [9]
Сероводород и углекислый газ активно взаимодействуют с компонентами технологических жидкостей с образованием сульфидов, сульфатов и карбонатов. При этом в растворе одновременно присутствуют молекулярный сероводород ( H2S) и ионы - бисульфид ( HS) и сульфид ( S), под воздействием которых может происходить деструкция реагентов стабилизаторов с потерей всех технологических свойств раствора. [10]
Химические методы заключаются в связывании растворенных в воде газов в новые химические соединения. Так, для более полного удаления молекулярного сероводорода и гидросульфидов из воды, применяются химические методы, основанные на их окислении и переводе в труднорастворимые соединения. [11]
Грачевой и Е. О. Барбакадзе ( см. табл. 15.6) установлено, что в корродированных в сероводороде образцах из минералов цементного клинкера, а также из индивидуальных гидратных фаз портландцемента, вопреки ожиданию, практически не содержатся сульфид-ионы, зато много элементной серы. Это обусловлено тем, что как собственно молекулярный сероводород, так и его соли являются сильными восстановителями и легко окисляются кислородом атмосферы и другими окислителями. [12]
Так, образование гидроксидов тяжелых металлов происходит при наличии избытка ионов ОН - за счет повышения рН воды. Примером взаимодействия серы с ионами Н при снижении рН может служить образование молекулярного сероводорода в кислой среде. [13]
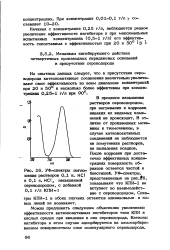 |
УФ-спектры погло-шения растворов 0 1 н. HCI и 0 1 н. HCI, насыщенной сероводородом, с добавкой О 1 г / л КПИ-1. [14] |
Катионы ингибитора в этом случае адсорбируются на хемосорбирр - ванном поверхностном слое молекулярного сероводорода. [15]
Страницы: 1 2