Золи - сера
Cтраница 2
Примерами гидрофильных золей, теряющих устойчивость лишь в концентрированных растворах электролитов, являются золи серы, оксидов и гидроксидов металлов и других соединений, дисперсная фаза которых сильно гидратирована за счет образования водородных связей с молекулами воды. Исследования стабильности и электрокинетического потенциала ряда гидрофобных золей ( галогенидов серебра, сульфидов мышьяка и сурьмы), к которым были добавлены неионогенные поверхностно-активные вещества ( оксиэтиЛированные эфиры этиленгликоля), показали, что образовавшиеся при этом дисперсии также представляют собой типичные лиофильные коллоидные растворы. Краснокутская и Сапон обнаружили, что с увеличением содержания ПАВ в растворе устойчивость золей в определенной области концентраций реагента возрастает настолько, что коагуляция наступает только в высококонцентрированных растворах - солей. Таким образом, гидратированные молекулы неионных ПАВ, адсорбируясь на гидрофобных коллоидных частицах, превращают их в гидрофильные. При действии электролитов с однозарядными противоионами очень малые добавки ПАВ вызывают эффект сенсибилизации. При коагуляции высокоустойчивых коллоидных растворов, стабилизированных ПАВ, заряд противоионов, как у всех гидрофильных золей, не имеет существенного значения. Гидрофилизи-рованный золь становится чувствительным к совместному действию дегидратирующих агентов ( например, этилового спирта или повышенных температур) и небольших количеств солей. Концентрация ПАВ, вызывающая превращение гидрофобного золя в гидрофильный, снижается с увеличением длины оксиэтиленовой цепи и углеводородного радикала молекулы ПАВ, но не связана с критической концентрацией мицеллообразования поверхностно-активного соединения. [17]
 |
Эффект Фарадея-Тиндаля. [18] |
Это подтверждается наблюдением / Например, при освещении золей белым ( смешанным) светом образующийся конус Фарадея - Тиндаля светится голубоватым цветом; золи серы, мастики и др. в отраженном свете кажутся голубоватыми; разбавленное молоко приобретает также синеватый оттенок. Голубой цвет неба и синий цвет морской воды объясняются также явлением светорассеяния. Различие окраски при рассматривании растворов в проходящем и отраженном свете, обусловленное светорассеянием, получило название опалесценции. [19]
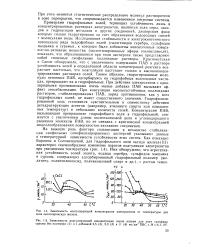
Из рис. 1 и 2 следует, чти введение в золи серы и селена небольших ( 10 - 3 - 10 - 5 моль / л) количеств спирта увеличивает степень извлечения дисперсной фазы с увеличением концентрации спирта в золе и его молекулярного веса. Введение в золи серы и селена больших количеств спирта ( 10 - 1 - 10 - 2 моль / л) резко увеличивает влажность пены и ее устойчивость, что делает невозможным использование метода пенообразования для выделения дисперсной фазы золей. Последнее хорошо согласуется с результатами опытов Скрылева и Мокрушина 17 ], исследовавшими влияние спиртов на процесс пенного выделения из гидрозолей коллоидных смешанных ферроцианидов тяжелых металлов. [20]
Введение в золи серы и селена небольших количеств этилового, бутилового и изоамилового спиртов оказывает благоприятное влияние на процесс пенного выделения дисперсной фазы. Введение в золи серы и селена больших количеств указанных выше спиртов резко увеличивает вспениваемость золей и делает невозможным использование метода пенообразования для выделения дисперсной фазы указанных золей. [21]
Из совершенно прозрачного коллоидного раствора серу можно осадить добавлением электролита; однако в большинстве случаев происходит только частичное выпадение серы, так как коллоидный раствор серы в противоположность коллоидным растворам металлов мало чувствителен к добавлению электролитов. Малые количества электролитов, прежде всего кислот, даже стабилизируют золи серы. Сера, выпадающая при добавлении электролитов, может быть обратно переведена в раствор при действии воды. [22]
Примером синтеза прямой конденсацией может служить получение золя ртути. Для этого Нордлунд пропускал пары ртути через слой воды и получал довольно высоко дисперсную эмульсию ртути в воде. Аналогичным способом могут быть получены золи серы, селена и теллура. Путем конденсации в жидкости паров меди, серебра, золота и платины, полученных в вольтовой дуге, можно получить соответствующие золи в воде, спиртах, глицерине или бензоле. Строение мицелл этих золей мало изучено. Стабилизатором при получении всех этих систем служат окислы веществ, получающиеся при соприкосновении их паров с воздухом при высокой температуре. Образование в таких условиях окислов, обладающих свойствами электролитов, подтверждается заметным возрастанием электропроводности системы. Однако более стойкие-золи получаются в том случае, если в воду, в которой происходит конденсация паров, вводят стабилизующие электролиты. [23]
Примером: синтеза прямой конденсацией может служить получение золя ртути. Аналогичным спосббом могут быть получены золи серы, селена и теллура. Путем конденсации в жидкости паров меди, серебра, золота и платины. Строение мицелл этих золей мало изучено. Стабилизатором при получении всех этих систем служат окислы веществ, получающиеся при соприкосновении их паров с воздухом при высокой температуре. Образование в таких условиях окислов, обладающих свойствами электролитов, подтверждается заметным возрастанием электропроводности системы. Однако более стойкие-золи получаются в том случае, если в воду, в которой происходит конденсация паров, вводят стабилизующие электроплиты. [24]
Доля рассеяния света, как следует из формулы, с большой длиной волны меньше, чем для лучей с малой длиной волны; так, например, красные или желтые лучи рассеиваются слабее голубых или фиолетовых. Отсюда следует, что при рассеянии белого света рассеянный свет должен получить голубоватый оттенок. Например, при освещении золей белым ( смешанным) светом образующийся конус Фарадея - Тиндаля имеет голубоватую окраску; золи серы, мастики и другие в отраженном свете кажутся голубоватыми; разбавленное молоко приобретает также синеватый оттенок. Голубой цвет неба и синий цвет морской воды объясняется явлением светорассеяния. Различие окраски при рассматривании растворов в проходящем и отраженном свете, обусловленное светорассеянием, получило название о п а л е с-ц е н ц ии. [25]
Установлено, что для золей металлов характерна селективность поглощения, зависящая от дисперсности. С ростом дисперсности максимум поглощения сдвигается в сторону коротких волн. Например, золи зо-ло Та, радиус частиц которых составляет около 20 нм, поглощают зеленую часть спектра ( - 530 нм), п поэтому они имеют ярко-красный цвет, при радиусе же частиц 40 - 50 нм максимум поглощения приходится на желтую часть спектра ( - 590 - 600 нм) и золь кажется синим. Кривые световой абсорбции золей серы по мере увеличения дисперсности также постепенно передвигаются к кривой абсорбции молекулярных растворов серы. Это подтверждает наличие непрерывного перехода некоторых свойств от дисперсных систем к истинным растворам. [26]
Золи с металлическими частицами очень сильно поглощают свет, что обусловлено генерацией в частицах электрического тока, большая часть энергии которого превращается в теплоту. Установлено, что для золей металлов характерна селективность поглощения, зависящая от дисперсности. С ростом дисперсности максимум поглощения сдвигается в область коротких воли. Например, золи золота, радиус частиц которых составляет - 20 им, поглощают зеленую часть спектра ( - 530 им), поэтому они имеют ярко-красную окраску, при радиусе частиц 40 - 50 им максимум поглощения приходится на желтую часть спектра ( - 590 - 600 нм) и такой золь золота кажется синим. Очень высокодисперсный золь золота, поглощая синюю часть спектра ( 440 - 450 нм), имеет желтую окраску, как и истинный раствор соли, например хлорида золота AuCls - Кривые световой абсорбции золей серы по мере увеличения дисперсности также постепенно приближаются к кривой абсорбции молекулярных растворов серы. Это подтверждает непрерывность некоторых свойств при переходе от дисперсных систем к истинным растворам. [27]
Страницы: 1 2