Золи - гидроокись - алюминий
Cтраница 2
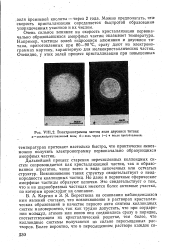 |
Электронограммы частиц золя двуокиси титана. а-свежеприготовленный золь. б-золь через 1 - 2 ч после приготовления.. [16] |
Очень сильное влияние на скорость кристаллизации первоначально образовавшихся аморфных частиц оказывает температура. Например, частицы золей гидроокиси алюминия и двуокиси титана, приготовленных при 80 - 90 С, сразу дают на электроно-граммах картину, характерную для мелкокристаллических частиц. [17]
Следует отметить, что золи гидроокиси алюминия, приготовленные при нагревании до 80 - 90, так же как и золи двуокиси титана, приготовленные в этих условиях, сразу дают на электронограммах картину мелкокристаллического вещества. Очевидно, и в случае золей гидроокиси алюминия при этих температурах процесс кристаллизации протекает настолько быстро, что практически невозможно заметить первоначально образующиеся аморфные частицы. [18]
Акустические исследования, основанные на измерении поглощения ультразвука, показывают перспективность изучения многих явлений, протекающих в микрогетерогенных коллоидных системах. Проведенные на технологическом объекте опыты по гидролитическому выделению золей гидроокисей алюминия или железа из гомогенного раствора с последующей коагуляцией этих золей в момент образования, а также пептизация коагелей могут быть непосредственно использованы как новая методика для контроля процессов очистки природных вод. До последнего времени не применялись инструментальные измерения для изучения явлений скрытой коагуляции коллоидных систем, представляющих собой начальную стадию макроскопических явлений визуально наблюдаемой коагуляции, а также определяющих их кинетику и окончательный результат. [19]
На многих водоочистительных станциях к воде, содержащей отрицательно заряженные органические примеси, добавляют положительно заряженные золи гидроокиси алюминия или железа. После взаимной коагуляции образовавшиеся хлопья легко отфильтровывают на песчаных фильтрах. [20]
На многих водоочистительных станциях к воде, содержащей отрицательно заряженные органические смеси, добавляют положительно заряженные золи гидроокиси алюминия или железа. После взаимной коагуляции образовавшиеся хлопья легко отфильтровываются на песчаных фильтрах. [21]
На многих водоочистительных станциях водопроводов поступают именно таким образом: к воде, содержащей отрицательно заряженные органические примеси, добавляют положительно заряженные золи гидроокиси алюминия или железа. После взаимной коагуляции образовавшиеся хлопья легко отфильтровывают на песчаных фильтрах. [22]
Потенциалообразующими ионами в первом случае служат ионы, образованные основными солями, вернее гидроксокомп-лексными ионами алюминия, а во втором - ионы водорода; противоионами в обоих золях являются хлор-ионы. Предполагается также существование мицелл гидроокиси железа со строением, аналогичным строению мицелл гидроокиси алюминия. Электрокинетический потенциал золей гидроокисей алюминия и железа положителен. Пептизация коагелей гидроокисей происходит при понижении рН среды, что может быть достигнуто простым добавлением исходной гидролизующейся соли. Этот процесс протекает по механизму диссолюции частиц с последующим образованием истинного раствора основных солей. [23]
Для исследования этого вопроса целесообразно использовать вискозиметрические измерения. Еще Робинерсон на очищенных золях А1 ( ОН) 3 и Fe ( OH) 3 показал, что коагуляция в данном случае сопровождается появлением аномальной вязкости в результате коагуляционного структуро-образования. Эдельман и Ребиндер при изучении тиксотропных свойств золей гидроокисей алюминия на приборе с коаксиальными цилиндрами установили, что гели гидроокиси алюминия, образующиеся в результате введения в золь электролитов-коагуляторов, являются упруго-пластично-вязкими телами с упругим последействием. [24]
В рассмотренных выше системах решающее значение имеют восстановительные или окислительные процессы, протекающие на поверхности коллоидных частиц, ибо стабилизирующие комплексы соответственных золей содержат ионы с переменной валентностью. Среди окисных гидрозолей существуют и такие, в которых металл, а следовательно и ионы, входящие в стабилизирующие комплексы, не имеют различных степеней окисления. Для выяснения вопроса о поведении таких систем при облучении было исследовано действие рентгеновских лучей на золи гидроокиси алюминия, существующего только в трехвалентном состоянии. [25]
Своеобразие коагулирования многовалентными ионами связано с процессом гидролиза. Во-вторых, для катионов А13 и Fe3 характерно образование соединений не только с ионами гидроксила, но и с ионизованными группами гидрофильных органических веществ: фосфатными, сульфатными, карбоксильными и др. В-третьих, предполагается, что с ростом рН среды от 4 до 7 увеличивается степень полимеризации гидроксокомплексов, и поэтому полиядерные формы соединений алюминия можно рассматривать как промежуточное звено между простыми ионами и полиэлектролитами. Отсюда следует, что отрицательно заряженные органические примеси могут связываться с продуктами гидролиза многовалентных ионов, и в этом состоит механизм снижения цветности. Кроме того, некоторые исследователи допускают существование флокуляции, вызванной полимерными комплексами ( полиэлектролитами), наподобие флокуляции высокомолекулярными соединениями. В-четвертых, при рН 5 - 7 5 преобладают нерастворимые продукты гидролиза, прежде всего золь А1 ( ОН) 3, а содержание растворимых форм ничтожно. Исследования гидроокиси алюминия показали, что первоначально образуются аморфные шарики размером 0 2 мкм, переход которых в кристаллическую форму протекает крайне медленно; но возможен дальнейший рост частиц, которые при рН 4 - 8 имеют в основном размер 2 мкм; при рН 8 5 - 9 3 преобладают частицы с размером 0 01 - 0 05 мкм. Золи гидроокисей алюминия и железа в дальнейшем превращаются в микрохлопья. В гелях Fe ( OH) 3 первичные частицы имеют размер 10 - 30 мкм. [26]
Своеобразие коагулирования многовалентными ионами связано с процессом гидролиза. Во-вторых, для катионов А13 и Fes характерно образование соединений не только с ионами гидроксила, но и с ионизованными группами гидрофильных органических веществ: фосфатными, сульфатными, карбоксильными и др. В-третьих, предполагается, что с ростом рН среды от 4 до 7 увеличивается степень полимеризации гидроксокомплексов, и поэтому полиядерные формы соединений алюминия моденр рассматривать как промежуточное звено между простыми ионами и подиэлект рд-литами. Отсюда следует, что отрицательно заряженные органические примеси могут связываться с продуктами гидролиза многовалентных ионов, и в этэм состоит механизм снижения цветности. Кроме того, некоторые исследователи допускают существование флокуляции, вызванной полимерными комплексами ( полиэлекТро - литами), наподобие флокуляции высокомолекулярными соединениями. В-четвертых, при рН 5 - 7 5 преобладают нерастворимые продукты гидролиза, прежде всего золь А1 ( ОН) 3, а содержание растворимых форм ничтожно. Исследования гидроокиси алюминия показали, что первоначально образуются аморфные шарики размером 0 2 мкм, переход которых в кристаллическую форму протекает крайне медленно; но возможен дальнейший рост частиц, которые при рН 4 - 8 имеют в основном размер 2 мкм; при рН 8 5 - 9 3 преобладают частацы с размером 0 01 - 0 05 мкм. Золи гидроокисей алюминия и железа в дальнейшем превращаются в микрохлопья. В гелях Fe ( OH) j первичные частицы имеют размер 10 - 30 мкм. [27]
Страницы: 1 2