Золь - иодид - серебро
Cтраница 1
Золь иодида серебра получен смешением равных объемов растворов иодида калия и нитрата серебра. [1]
Сначала рассмотрим золь иодида серебра, находящийся в равновесии с асыщенным раствором. Концентрации ионов серебра и иода в растворе фактически равны, хотя сами частицы благодаря преимущественной адсорбции ионов ода заряжены отрицательно. [2]
Образуется голубоватый опалесцирующий золь иодида серебра. [3]
В проходящем свете золь иодида серебра имеет оранжево-красный цвет, в отраженном - голубой. [4]
При этом образуется слегка опалесцирующий золь иодида серебра. Этот золь наливают в кювету с плоскопараллельными стенками и освещают пучком яркого света от проекционного фонаря, как это уже было описано в предыдущих опытах. [5]
ЛО 4 М) образуется золь иодида серебра. [6]
KI разбавляют до 100 мл водой и к разбавленному раствору добавляют при взбалтывании 10 капель 1 7 % - ного раствора AgNOa - Образуется голубоватый опалесцирующий золь иодида серебра. [7]
Устойчивость золя зависит от электрического заряда его дисперсной фазы. Если золь иодида серебра приготовляется из нитрата серебра прибавлением к нему в избытке иодида калия, то частицы иодида серебра остаются коллоидными потому, что они способны адсорбировать Л - - ионы. В результате такой адсорбции поверхность частиц AgJ становится отрицательно заряженной. Вокруг этих частиц распределяется эквивалентное количество положительных ионов, так что весь раствор в целом остается электронейтральным. Так образуется диффузионный двойной электрический слой, свойства которого определяют стабильность этой системы. [8]
KI разбавляют до 100 мл водой и к разбавленному раствору добавляют при взбалтывании 10 капель 1 7 % - ного раствора AgNOs. Образуется голубоватый опалесцирующий золь иодида серебра. [9]
Например, золь иодида серебра, полученный в результате взаимодействия нитрата серебра и иодида калия, всегда содержит значительное количество индифферентного электролита - нитрата калия. В других случаях электролиты и иные низкомолекулярные примеси могут попадать в коллоидные системы вследствие загрязненности исходных продуктов или по другим причинам. [10]
Коагулирующиеся мицеллы золя сохраняют на себе те ионы, которые придавали им первоначальный заряд. Так, например, отрицательно заряженный золь иодида серебра устойчив потому, что его частицы адсорбируют Т - - ионы. [11]
Для аналитической химии важно, что стабилизирующий ион, который определяет заряд золя, всегда адсорбируется при коагуляции. Если к раствору иодида мы прибавим нитрат серебра, то образуется золь иодида серебра, который обязан своей устойчивостью адсорбированным иодид-ионам. [12]
Машинное ( или растительное) масло. Растворы: щелочи ( 20 % - ный), мыла ( 2 % - ный), канифоли ( насыщенный спиртовой) или серы, фенолфталеина, желатина ( 0 5 % - ный, насыщенный), жидкого стекла ( пл. Золь иодида серебра, полученный: а) в избытке иодида калия, б) в избытке нитрата серебра. [13]
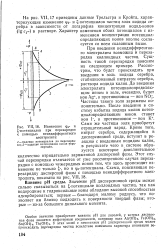 |
Изменение q0 - и - потенциалов при перезарядке с помощью неиндифферентного. [14] |
При введении неиндифферентного электролита возможна и перезарядка коллоидных частиц. Сущность такой перезарядки поясним на следующем примере. Рассмотрим, что будет происходить при введении в золь иодида серебра, стабилизованный нитратом серебра, раствора иодида калия. До введения электролита потенциалопределяю-щим ионом в золе, очевидно, будет ион Ag, а противоионом - ион NOj. Частицы такого золя заряжены положительно. После введения в систему избытка иодида калия потен-циалопределяющим ионом станет ион 1 -, а противоионом - ион К - Сами же частицы золя приобретут отрицательный заряд. [15]
Страницы: 1 2