Взаимодействие - молекула - спирт
Cтраница 1
 |
Адсорбция молекулы в последнее время А. А. Баландин. [1] |
Взаимодействие молекулы спирта со свободной валентностью поверхности приводит к хемосорбции радикала ( СНзЬСНО и атома подорода, который связывается с атомом водорода, находившимся при вторичном атоме углерода. Образовавшийся радикал СН3СОСНз десорбирустся, образуя молекулу ацетона. [2]
 |
Дегидрогенизация изопропилового спирта. [3] |
Взаимодействие молекулы спирта со свободной валентностью поверхности приводит к хемосорбиии радикала ( СН3) гСНО и атома водорода, который связывается с атомом водорода, находившимся при вторичном атоме углерода. Образовавшийся радикал СН3СОСНз десорбируется, образуя молекулу ацетона. [4]
 |
Схема дегидрогенизации изопропилового спирта. [5] |
Взаимодействие молекулы спирта со свободной валентностью поверхности приводит к хемосорбции радикала ( СН3) 2СНО и атома водорода, который связывается с атомом водорода, находящимся при вторичном атоме углерода. Образовавшийся радикал СН3СОСН3 десорбируется, образуя молекулу ацетона. Легко видеть, что изменение температуры, введение кислорода или другие воздействия, изменяющие концентрацию электронов в зоне проводимости полупроводника, должны в таких случаях одновременно изменять и электропроводность, и каталитическую активность его. [6]
 |
Адсорбция молекулы в последнее время А. А. Баландин. [7] |
Взаимодействие молекулы спирта со свободной валентностью поверхности приводит к хемосорбции радикала ( СН3ЬСНО и атома водорода, который связывается с атомом водорода, находившимся при вторичном атоме углерода. Образовавшийся радикал СН3СОСНз десорбируется, образуя молекулу ацетона. [8]
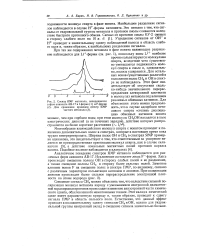 |
Спектр ЯМР метанола, находящегося. [9] |
Многообразие взаимодействия молекул спирта с ионитом приводит к появлению дополнительных полос в спектрах, которые в настоящее время пока трудно интерпретировать. Ширина полос ОН и СН3 в спектрах ЯМР примерно одинакова, это свидетельствует о том, что ответственным за уширение является не преимущественная ориентация молекул спирта, как в случае сили-кагеля [3], а действие локальных магнитных полей протонов каркаса ионита. [10]
Значительное смещение полосы ассоциированных молекул показывает, что взаимодействие молекул спирта с молекулами растворителя, имеющего атом кислорода, настолько сильно, что имеет характер ассоциации этих молекул. Этот тип ассоциации конкурирует с ассоциацией молекул спирта друг с другом. Подобная интерпретация наблюдаемых изменений в спектрах комбинационного рассеяния подтверждается исследованием тройных смесей [315, 316] Выше указывалось, что в 2 % - ном растворе метилового спирта в СС14 наблюдаются интенсивная линия изолированных молекул и слабая полоса ассоциированных молекул спирта. Если к этой смеси добавить несколько процентов ацетона, то спектр изменяется: интенсивность линии изолированных молекул резко уменьшается, и появляется полоса с частотой 3530 см 1, принадлежащая группам ОН спирта, взаимодействующим с атомом кислорода ацетона. [11]
Это свидетельствует о том, что с увеличением температуры ослабляется взаимодействие молекул спиртов с полярной неподвижной жидкой фазой в большей степени, чем взаимодействие соответствующих им альдегидов. [12]
 |
Я. Концентрационная зависимость. С в системах С jHgOH - метилцнклогексаи ( - и С2Н5ОН - толуол ( - -. [13] |
При взаимодействии молекул спирта друг с другом главным является образование Н - связей, приводящее к ассоциации молекул в чистом спирте. [14]
Оказалось, что взаимодействие молекул спирта с ионом металла в сольватном комплексе не ограничивается зоной гидро -, ксила, который, по-видимому, непосредственно связан с катионом, а распространяется по всей молекуле спирта, что выражается не только в сдвиге линий ОН, но и линий алкила. Авторы объясняют это явление тем, что в комплексе происходит соответствующая делокализация неспаренных электронов катиона. [15]
Страницы: 1 2