Взаимодействие - ниобий
Cтраница 1
Взаимодействие ниобия с молибденом начинается при температуре 1100 С. С повышением температуры коэффициент адгезии резко возрастает, а при 1300 С образуется сварное соединение, разрушающееся по плоскости контакта. Борирование ниобия повышает температуру начала адгезионного взаимодействия с молибденом на 200, а карбидизация - на 100 С. В случае силици-рования ниобия температура начала взаимодействия его с молибденом не изменяется. С повышением температуры значения коэффициента адгезии возрастают, однако склонность к схватыванию ниже, чем для пары ниобий-молибден. [1]
Особенностью взаимодействия ниобия с ПАР является то, что в присутствии третьих компонентов ( тартрат -, оксалат -, фторид-ионов, пероксида водорода, комплексо-на III) образуются тройные ( или смешанные) комплексные соединения. [2]
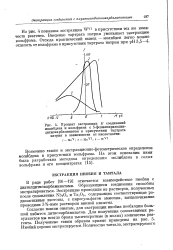
При изучении реакции взаимодействия ниобия с ПААК и его бромпроизводными сначала было проверено влияние лигандов, обычно применяемых для перевода этого элемента в раствор и разрушения его полиядерных соединений. Опыты показали, что наиболее устойчивые соединения со всеми синтезированными реагентами, в том числе и с ПААК, ниобий образует в присутствии тар-трат-ионов, и все дальнейшие опыты проводились в тартратной среде. На рис. 1 приведены кривые зависимости оптической плотности комплексов ниобия с ПААК и его бромпроизводными от рН среды. [3]
Метод основан на взаимодействии ниобия ( V) с рода-нистоводородной кислотой в солянокислом растворе с образованием комплексного соединения Н [ NbO ( SCN) 4 ], окрашенного в желтый цвет. Образующийся комплекс экстрагируют эфиром или определяют содержание ниобия в гомогенной водно-ацетоновой среде. [4]
Какие продукты получаются при взаимодействии ниобия и тантала с хлористым водородом. [5]
 |
Процент экстракции Е соединений. [6] |
В ряде работ [16-19] отмечается взаимодействие ниобия с диэтилдитиокарбаминатами. Образующиеся соединения способны экстрагироваться. [7]
Фосфид ниобия NbP был получен в результате взаимодействия ниобия с фосфором при 500 в запаянной эвакуированной трубке. [8]
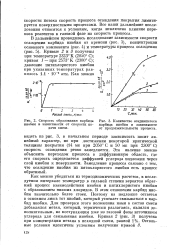 |
Скорость образования карбида ниобия в зависимости от скорости подачи смеси.| Количество осадившегося карбида ниобия в зависимости от продолжительности процесса. [9] |
Как можно убедиться из термодинамических расчетов, в исследуемом интервале температур в сильной степени вероятен обратный процесс взаимодействия ниобия и пятихлористого ниобия с образованием низших хлоридов. В этом отношении карбид ниобия значительно более стоек. Поэтому на подложке остается в основном лишь тот ниобий, который успевает связываться в карбид ниобия. Для проверки этого положения нами в состав смеси добавлялся метан, который, термически разлагаясь, являлся дополнительным, но поступающим уже из газовой фазы источником; углерода для связывания ниобия. [10]
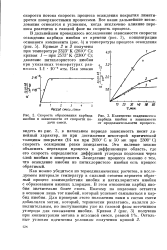 |
Скорость образования карбида ниобия в зависимости от скорости подачи смеси.| Количество всадившегося карбида ниобия в зависимости от продолжительности процесса. [11] |
Как можно убедиться из термодинамических расчетов, в исследуемом интервале температур в сильной степени вероятен обратный процесс взаимодействия ниобия и пятихлористого ниобия с образованием низших хлоридов. В этом отношении карбид ниобия значительно более стоек. Поэтому на подложке остается в основном лишь тот ниобий, который успевает связываться в карбид ниобия. Для проверки этого положения нами в состав смеси добавлялся метан, который, термически разлагаясь, являлся дополнительным, но поступающим уже из газовой фазы источником углерода для связывания ниобия. [12]
Для определения ниобия наиболее чувствительным и универсальным методом является роданидный. Метод основан на взаимодействии ниобия с роданистоводородной кислотой с образованием желтого комплекса. Тантал в тех же условиях образует бесцветный комплекс. [13]
Режимы получения достаточно плотных, прочно сцепленных с основой защитных покрытий на ниобии и их характеристика приведены в таблице. Судя по изменению коэффициента адгезии с температурой, взаимодействие ниобия с незащищенным ниобием начинается при 1100 С. С повышением температуры коэффициент адгезии возрастает, достигая при 1300 С значения 0.37. Карбидизация и силицирование ниобия повышают температуру начала адгезионного взаимодействия на 100 С, а борирование - на 200 С. В случае защиты обеих контактирующих поверхностей [7] борирование также более эффективно уменьшает склонность ниобия к схватыванию, чем карбидизация. [14]
В вышеуказанных исследованиях для определения наличия NbsSn структуру обычно определяли методом рентгеноструктур-ного анализа. Пикклесимер с помощью микроструктурного анализа доказал, что в результате взаимодействия ниобия и олова при высоких температурах образуются и другие фазы. [15]
Страницы: 1 2