Взаимодействие - окись - алюминий
Cтраница 1
Взаимодействие окиси алюминия с нелегированным титаном и сплавом Ti - 6Al - 4V в интервале температур 923 - 1144 К исследовали Тресслер и Мур [46]; они показали, что в реакционном слое образуется соединение Ti3Al с низким содержанием кислорода. В связи с этим были подвергнуты исследованию как кинетика роста указанной фазы, так и растворение кислорода в матрице. Более подробно эти вопросы рассмотрены в гл. [1]
Взаимодействие окиси алюминия с углеродом до 1650 С протекает в небольшой степени. С ростом температуры и появлением жидкой фазы взаимодействие резко усиливается. Образование жидкой фазы способствует ускорению процесса. Основным конденсированным продуктом восстановления на этой стадии является карбид алюминия, содержание которого возрастает до 1950 С. Металлический алюминий появляется при 1900 С. [2]
Взаимодействие окиси алюминия с углеродом в этих условиях протекает через образование оксикарбидов состава Al. При контакте в течение 2 ч графита с термопарными сплавами копель и алюмель в вакууме 5 - 10 - 3 мм рт.ст. взаимодействие не обнаруживается и при температуре 1100 С, в то время как с хромелем в этих же условиях наблюдается некоторое увеличение микротвердости на границе контакта. [3]
Получается взаимодействием окиси алюминия с серной кислотой. Нефелиновый коагулянт получается обработкой нефелина серной кислотой. [4]
Таким образом, взаимодействие окиси алюминия с концентрированными растворами HF приводит к образованию новых химических соединений: гидроксофторидов алюминия или их смесей с фтористым алюминием. [5]
 |
Вид двуслойного покрытия грунтовая эмаль 2015 / 3132-окись алюминия. [6] |
При последующем нагреве начинается взаимодействие окиси алюминия с эмалью. [7]
СггОз с цезием интенсивность взаимодействия окиси алюминия, содержащей эти примеси, с парами цезия должна возрастать. [8]
Для облегчения перерождения силиманита и андалузита, ускорения взаимодействия окиси алюминия с глиной для образования муллита и снижения температуры обжига, в состав массы вводят от 3 до 5 % плавней. [9]
Рассчитаны приращения энтальпии, энтропии и изобарно-изо-термического потенциала реакций взаимодействия окиси алюминия с окислами бериллия, магния, кальция, стронция и бария; оценены энтальпия, энтропия и потенциал Гиббса образования моноалюминатов элементов второй группы. [10]
Аккерман и Торн ( Ackermann, Thorn, 1958) подробно рассмотрели взаимодействие окиси алюминия, окиси магния, двуокиси урана, двуокиси тория, окиси бериллия и двуокиси циркония с вольфрамом и танталом, из которых обычно изготовляются эффузионные ячейки. [11]
Указанная температура достигается за счет физического тепла нагретых гранул, а также тепла экзотермической реакции взаимодействия окиси алюминия с серной кислотой. В процессе выщелачивания в раствор переходят сульфат алюминия и алюминиевые квасцы. Железо, присутствующее в концентрате, также взаимодействует с серной кислотой и переходит в раствор. [12]
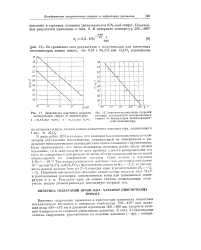 |
Зависимость константы скорости дегидратации спирта от температуры.| Зависимость константы скорости. [13] |
В ряде работ [10] показано, что активность алюмосиликатных катализаторов обусловлена кислотностью, возникающей на поверхности в результате топохимического взаимодействия окиси алюминия с кремнеземом. [14]
Термодинамический анализ этой реакции показывает [1], что в атмосфере, содержащей треххлсристый фосфор, возможна пайка алюминия, поскольку при температуре выше 182 С все продукты взаимодействия окиси алюминия А12О3стреххлористым фосфором находятся в газообразном состоянии. [15]
Страницы: 1 2