Взаимодействие - торий
Cтраница 1
Взаимодействие тория с водными растворами кислот имеет любопытные особенности. Плавиковая кислота покрывает металл защитной фторидной пленкой. Аналогичное пассивирующее действие оказывает концентрированная HNO3, но добавление иона фтора снимает пассивность. Разбавленные HNO3, H2SO4 и HF, а также концентрированная Н3РС4 взаимодействуют с торием медленно [99]; НС1 растворяет металл довольно энергично, но не до конца. [1]
Взаимодействием тория с галоидами ( I, Вт, С1) при определенных условиях ( состава и температуры) были синтезированы га лиды ТЬГз и ТЬГа. С), обладающие хорошей электропроводностью и при взаимодействии с кислотами выделяющие водород. Нагревание этого вещества ( в отсутствие воздуха) выше 880 С сопровождается его дисмутацией но схеме: 2Thl2 ThI. Теплоты образования из элементов This и Т1тС1з оцениваются соответственно в 156 и 190 ккал / моль. [2]
При взаимодействии тория с фитиновой кислотой [173] в кислых растворах образуется трудиорастворимое соединение. [3]
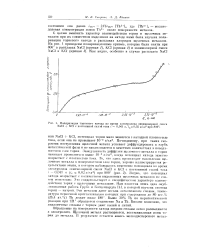 |
Поляризация ториевого катода во время электролиза эквимолярнои смеси NaCl KC1 с постоянной сплои тока i 0 041 я, г кгО 02 а / см2 при 806. [4] |
С целью выяснить характер взаимодействия тория и щелочных металлов при их совместном выделении на катоде нами была изучена поляризация ториевого катода в расплавах хлоридов щелочных металлов. [5]
Этот метод2 основан на реакции взаимодействия тория с реагентом тороном в минеральнокислой среде, в результате которой образуется красно-малиновый осадок, а в случае разбавленных растворов-розовое окрашивание. Кузнецова, в солянокислых или азотнокислых растворах окрашенные соединения с реагентом, помимо тория, образуют только цирконий, гафний и титан. Редкоземельные элементы не дают цветной реакции с тороном в минерально-кислой среде, но при значительной их концентрации в растворе может иметь место некоторое изменение окраски реагента. [6]
Этот метод 2 основан на реакции взаимодействия тория с реагентом тороном в минеральнокислой среде, в результате которой образуется красно-малиновый осадок, а в случае разбавленных растворов - розовое окрашивание. По данным В. И. Кузнецова, в солянокислых или азотнокислых растворах обкрашенные соединения с реагентом, помимо тория, образуют только цирконий, гафний и титан. [7]
Гердс и Маллет изучали также реакцию взаимодействия тория с азотом при атмосферном давлении. [8]
Изучение состава соединения, образующегося при взаимодействии тория с тороном, по метолу Остромысленского, показало, что они реагируют в отношении 1: 2, причем в реакцию вступают ионы Th4 и двухвалентные анионы, получающиеся при кислотной диссоциации реагента. [9]
Иначе ведет себя торий. При взаимодействии растворов солей тория и хромооксалата калия выделяется оксалат тория благодаря взаимодействию тория с внутрисферными оксалат-ионами. Реакция с хромооксалатом позволяет изолировать самарии и отделить торий. [10]
Иначе ведет себя торий. При взаимодействии растворов солей тория и хромооксалата калия выделяется оксалат тория благодаря взаимодействию тория с внутрисферными оксалат-ионамп. Реакция с хромооксалатом позволяет изолировать самарий и отделить торий. [11]
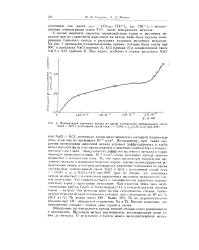 |
Поляризация ториевого катода во время электролиза эквимолярнои смеси NaCl KC1 с постоянной сплои тока i 0 041 я, г кгО 02 а / см2 при 806. [12] |
По-видимому, при таких скоростях поступления щелочной металл успевает диффундировать в глубь металлической фазы и но накапливается в заметных количествах в поверхностном слое тория. Замедленность диффузии щелочного металла в тории начинает проявляться выше 10 - 2 а / см2, когда потенциал катода заметно возрастает с плотностью тока. Это свидетельствует о специфическом характере взаимодействия тория с щелочными металлами. Нам известна лишь одна опубликованная работа Грубе и Ботцснгардта [4], в которой изучена система торий - натрий. [13]
Страницы: 1