Алюминий-триалкила
Cтраница 1
Алюминий-триалкилы ( за немногим исключением) ассоциированы до ди-меров. Таким образом, в сумме затрачивается энергия ( UАХ 10) ккал. [1]
Алюминий-триалкилы ( за немногим исключением) ассоциированы до ди-меров. Таким образом, в сумме затрачивается энергия ( с / АХ Ю) ккал. [2]
Обычно алюминий-триалкилы или диалкилалюминийгидриды высокой чистоты приготовляются из триизобутилалюминия. [3]
Очень трудно, если вообще возможно, получить алюминий-триалкилы в чистом виде. Установление равновесия происходит в рассмотренных выше случаях уже при 50 довольно быстро. Если олефины имеют высокую температуру кипения, то даже и в самом высоком вакууме выделить чистые алюминийтриалкилы не удается. Результат может быть улучшен с помощью непрерывной пленочной дистилляции, но несущественно. Этот вывод сделан сначала лишь для алюминийтриалкилов с а-разветвлен-ными первичными радикалами. Само собой разумеется, что соотношения более благоприятны у соединений с нормальными алкильными радикалами у алюминия. [4]
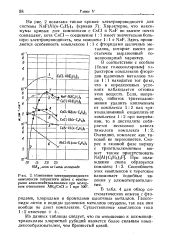 |
Изменение электропроводности комплексов хлористого цезия с некоторыми алюминнйтриалкилами при молярном отношении AlR3 / CsCl 1 при 100. [5] |
Из данных таблицы следует, что по отношению к алюминий-триалкилам хлористый рубидий является более сильным комп-лексообразователем, чем бромистый цезий. [6]
Хлориды и бромиды ввиду малой разности температур кипения отогнаны быть не могут и для их отделения приходится пользоваться иными способами, напр имер превращением в алюминий-триалкилы под действием металлического натрия или в комплексные соединения, не смешивающиеся с алюминийтриалкилами при действии хлористого или бромистого калия. [7]
В момент разрыва ас-социаты, 1как более реакционноапособные, в первую очередь подвергаются дальнейшим превращениям. В мономерных алюминий-триалкилах с разветвленными радикалами, например в триизобу-тилалюминии, внутренняя стабилизация осуществляется за счет собственной разветвленной алкильной группы, и, поскольку не затрачивается энергия на диссоциацию молекул, термостойкость их значительно ниже, чем у ассоциированных молекул. [8]
Как только весь изобутилен отогнан, добавляют оставшееся количество олефина, охлаждают реакционную смесь до 60 С и выдерживают ее в течение нескольких часов. В результате получают практически чистые алюминий-триалкилы, свободные от продуктов димеризации, но в них всегда присутствуют изобутилпроизводные алюминия. [9]
Однако практическое применение алюминийтриалкилов не исчерпывается только каталитическими системами. За последнее время алюминий-триалкилы широко используют для промышленного синтеза высших жирных спиртов. В этом случае смесь алюминийтриалкилов с оле-финами окисляют воздухом; в результате образуются алкоголяты алюминия, которые при взаимодействии с водой разрушаются с образованием окиси алюминия и первичных жирных спиртов. При тщательном контроле можно обеспечить условия для преимущественного образования какого-либо одного продукта, в связи с этим процесс приобретает особую важность для промышленного производства моющих средств. [10]
Для получения индивидуальных алюминийалкилов могут быть использованы методы синтеза триэтил - и триизобутилалюминия [29, 44], но условия проведения реакций еще недостаточно определены, особенно для получения алюминийалкилов с прямой углеродной цепью. Конечными продуктами при таком способе в зависимости от того, на какой стадии остановить процесс, могут быть алюминий-триалкилы и диалкилалюминийгидриды. В случае получения диал-килалюминийгидридов в реакционной смеси остается небольшое количество триалкилалюминия в виде примеси. Для получения более чистого диалкилалюминийгидрида ( практически без примесей A1R3) необходимо в течение нескольких часов нагревать реакционную смесь до 140 - 160 С в присутствии водорода. [11]
При получении триэтил - и трипропилалюминия из изобутил-ялюминиевых соединений очень полезно пользоваться следующим приемом. Из продажного триизобутилалюминия можно легко получить триэтил - и трипропилалюминии, для чего в начале реакции следует добавить немного ацетилацетоната никеля и ввести при 50 - 100 этилен или пропилен. В конце процесса алюминий-триалкил с целью освобождения его от никеля перегоняют под вакуумом. [12]
При обычных температурах эта реакция не идет. Выше температуры плавления натрия ( 120 - 130е) реакция идет энергично. Образующиеся натрийалюминийтетраалкилы нерастворимы в алюминий-триалкилах и выделяются в виде жидкого нижнего слоя, который при охлаждении застывает. [13]
Другие методы получения алюминийтриалкилов и алкил-алюминийгидридов основаны на реакциях взаимного вытеснения олефинов в триалкилах и присоединения олефинов к связи алюминий-водород. При проведении этих реакций не требуется применения тонкоизмельченного алюминия, однако и им свойственны другие приведенные выше для прямого синтеза недостатки. Кроме того, компонентами этих реакций являются алюминий-триалкилы, алкилалюминийгидриды, алюминийгидрид или ли-тийалюминийгидрид, являющиеся в свою очередь продуктами тонкого химического синтеза. [14]
Конечным продуктом реакции является смесь алюминийтриалки-лов, при взаимодействии которой с водой получаются н-алканы, содержащие четное число углеродных атомов. Длина алкильной цепи зависит от числа прореагировавших молекул этена. Для получения алю-минийтриалкилов, содержащих нечетное число углеродных атомов, применяли [118, 123] трипропилалюминий; синтезировать алюминий-триалкилы с нечетным числом углеродных атомов, используя триметил-алюминий, невозможно. [15]
Страницы: 1