Притягательное взаимодействие
Cтраница 1
Притягательные взаимодействия между специфически адсорбированными на ртути изотиоцианатными комплексами Cr ( III) могут определяться и притягательными взаимодействиями между входящими в их состав специфически. [1]
При очень сильном притягательном взаимодействии между органическими катионами и специфически адсорбированными анионами возможно образование конденсированных поверхностных слоев. [2]
Силы, обусловленные притягательным взаимодействием противоположно заряженных тел. [3]
Положительная аттракционная постоянная означает притягательное взаимодействие в адсорбционном слое и соответствует его уплотнению и возрастанию защитных свойств. [4]
Эти силы отличаются от чисто притягательных взаимодействий глинистых частиц, которые, согласно измерениям Уиттакера, определяют пределы пластичности в разбавленных суспензиях. Они гораздо выше последних, что видно по значительно большей крутизне кривой зависимости предела пластичности от концентрации при переходе от разбавленных суспензий к концентрированным смесям ( фиг. [5]
Положительное значение аттракционной постоянной характеризует притягательное взаимодействие молекул соединений в адсорбированном слое. При этом происходит мономолекулярное заполнение поверхности. [6]
Наиболее чувствительной является форма С ф-кривой к притягательному взаимодействию между адсорбированными молекулами. При сильном притягательном взаимодействии между вертикально ориентированными молекулами ( аи 1 3), что имеет место при адсорбции кумарина на Hg и Bi, и в случае а22 а 2 О наблюдается относительно высокий максимум переориентации при фво. По расположению и высоте этот максимум напоминает пик переориентации на С, ф-кривой ртути. Увеличение а22 без изменения а ] 2 приводит к резкому возрастанию высоты этого максимума. Этот эффект отражает ослабление различий в двух положениях, которые могут занимать молекулы адсорбата на поверхности висмутового электрода. [7]
Физической основой падения активности по сравнению с концентрацией является притягательное взаимодействие частиц. Взаимное отталкивание частиц в растворе должно, наоборот, вызывать увеличение активности. В разбавленных растворах электролитов электростатическое притяжение ионов оказывается преобладающим: v l и падает с ростом концентрации. Учет собственного размера ионов эквивалентен учету сил отталкивания, не позволяющих ионам сблизиться на расстояние, меньшее а. Второе приближение теории, учитывающее этот фактор, приводит к менее резкому уменьшению коэффициента активности ( рис. 10) и позволяет описать опытные данные в более широком интервале концентраций. Однако в концентрированных растворах большая часть молекул воды связана ионами, так что добавление новых порций электролита должно сопровождаться разрушением сольватных оболочек и преодолением сил ион - диполь-ного взаимодействия. [8]
Отталкивательное взаимодействие, существующее, между одноименно заряженными органическими катионами в поверхностном слое, сменяет притягательное взаимодействие между гало-генид-анионами и органическими катионами при совместной адсорбции. Это приводит к упрочению связи и уплотнению адсорбционной пленки. По такому механизму, по мнению Л. И. Антропова, действуют смеси пиридиновых производных и галогенид-ионов. [9]
Притягательные взаимодействия между специфически адсорбированными на ртути изотиоцианатными комплексами Cr ( III) могут определяться и притягательными взаимодействиями между входящими в их состав специфически. [10]
Аттракционная постоянная а здесь характеризует межмолекуляр-ное взаимодействие компонентов А и В в поверхностной фазе: она тем больше, чем сильнее парные притягательные взаимодействия А-А, В-В, и тем меньше, чем сильнее притягательное взаимодействие А-В. Следует подчеркнуть, что такая трактовка изотермы Фрумкина не совсем верна, поскольку толщина адсорбционного слоя не обязательно должна оставаться постоянной в процессе адсорбции. [11]
Аттракционная постоянная а здесь характеризует межмолекуляр-ное взаимодействие компонентов А и В в поверхностной фазе: она тем больше, чем сильнее парные притягательные взаимодействия А-А, В-В, и тем меньше, чем сильнее притягательное взаимодействие А-В. Следует подчеркнуть, что такая трактовка изотермы Фрумкина не совсем верна, поскольку толщина адсорбционного слоя не обязательно должна оставаться постоянной в процессе адсорбции. [12]
Они показали, что при переходе от сульфатного к кислому иодидному раствору ( серная кислота с добавкой иодида калия) изотерма адсорбции катиона децилпиридиния приобретает S-образный вид, причем отталкивание в адсорбционном слое сменяется сильным притягательным взаимодействием. Это обусловлено тем, что в присутствии иодида калия адсорбция органического катиона идет по слою специфически адсорбированных анионов и сопровождается сильным притягательным взаимодействием между разноименно заряженными частицами. [13]
Будем предполагать, что члены г - 6, связанные с индуцированными квадруполями, в среднем также аддитивны, так что их можно объединить с дисперсионными членами в W В результате для каждой пары ионов получается притягательное взаимодействие, обратно пропорциональное шестой степени расстояния, с численным коэффициентом, учитывающим возмущения обоих типов. [14]
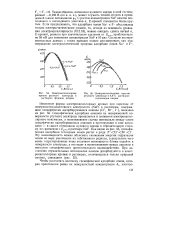 |
Электрокапиллярные кривые. [15] |
Страницы: 1 2