Внутримолекулярное взаимодействие - группа
Cтраница 1
Аналогичное внутримолекулярное взаимодействие групп NO2 и СООН в о-нитробензойной кислоте не наблюдается, так как в этом соединении атом водорода группы СООН находится на большем расстоянии от нитрогруппы, чем атом водорода группы ОН в о-нитрофеноле. [1]
Аналогичное внутримолекулярное взаимодействие групп NOz и СООН в а-нитробензойной кислоте не наблюдается, так как в Этом соединении атом водорода группы СООН находится На большем расстоянии от нитрогруппы, чем атом водорода группы ОН в о - ргнтро феноле. [2]
Для осуществления внутримолекулярного взаимодействия нит рильных групп в динитрилах, содержащих восемь и более атомов углерода в основной цепи, используется принцип разбавления Руггли - Циглера 55 - ш, ш - 17б Поскольку в указанных динитрилах благодаря стерическим факторам межмолекулярное взаимодействие функциональных групп протекает значительно быстрее, чем внутримолекулярное взаимодействие, реакцию проводят в сильно разбавленных растворах. При этом вероятность замыкания кольца остается той же, как и в сравнительно концентрированных растворах, а вероятность бимолекулярного взаимодействия динитрилов резко уменьшается. Практически, значительное разбавление достигается тем, что подлежащее циклизации соединение медленно подается в реакционный сосуд, в котором поддерживаются необходимые для проведения реакции условия. [3]
В заключительной главе 21 обсуждаются различные виды внутримолекулярного взаимодействия групп. Целесообразно рассматривать все бесчисленные случаи замыкания колец, при которых получаются алициклические, конденсированные ароматические или гетероциклические системы, не как нечто особое, а как простой внутримолекулярный вариант изученных ранее межмолекулярных реакций. На мой взгляд, знакомство с такими внутримолекулярными взаимодействиями следует начинать уже на ранней стадии изучения органической химии, поскольку они играют важную роль в биохимии и в теориях биосинтеза. [4]
В заключительной главе 21 обсуждаются различные виды внутримолекулярного взаимодействия групп. Целесообразно рассматривать все бесчисленные случаи замыкания колец, при которых получаются алициклические, конденсированные ароматические или гетероциклические системы, не как нечто особое, а как простой внутримолекулярный вариант изученных ранее межмолекулярных реакций. На мой взгляд, знакомство с такими внутримолекулярными взаимодействиями следует начинать уже на ранней стадии изучения органической химии, поскольку вни играют важную роль в биохимии и в теориях биосинтеза. [5]
Небольшие изменения характеристических частот колебаний группы обусловлены локальными отличиями в структуре молекулы вследствие или внутримолекулярного взаимодействия групп, или межмолекулярного взаимодействия с окружающими молекулами. [6]
Влияние строения динитрила на направление реакции восстановления заключается, по-видимому, в изменении соотношения скоростей конкурирующих реакций - гидрирования альдимина и внутримолекулярного взаимодействия альдиминной группы с первичной аминной. В случае гидрирования алифатических а со-динитрилов с 7 - 12 атомами углерода в цепи, а также мета - и пара-замещенных ароматических динитрилов преобладает гидрирование альдимина и циклизации не происходит. При восстановлении динитрилов с двумя атомами углерода между нитрильными группами преобладает второе направление реакции - образование циклического продукта. Из этих данных следует, что решающее влияние на направление процесса оказывает строение молекулы динитрила. [7]
Именно внутримолекулярное образование водородной связи приводит к наиболее важным стереохимическим последствиям; неудивительно, что первоначальное открытие водородной связи и развитие представлений о ней были связаны с наблюдениями внутримолекулярного взаимодействия групп. Образование водородной связи в молекуле ( приводящее к образованию клешневидного цикла) вызывает два важных следствия; во-первых, подавляется ассоциация молекул благодаря внутримолекулярной занятости атома водорода, обусловливающего ассоциацию; во-вторых, снижается нормальная химическая активность группы, содержащей этот водородный атом. [8]
Первичным актом реакции является присоединение О-нуклеофильного центра ( или S -, N-нуклеофила HXCt Ct RYH) этиленгликоля по двойной связи с образованием карбаниона В, который может стабилизироваться элиминированием фторид-иона либо от группы a - CF, либо от группы a - СРз. Затем внутримолекулярное взаимодействие группы НО или алкоксианиона с электрофильным центром молекул и приводит к 5-членному и 7-членному гетероциклам. Соотношение этих гетероциклов существенным образом зависит от природы используемого растворителя и нуклеофильного реагента. [9]
 |
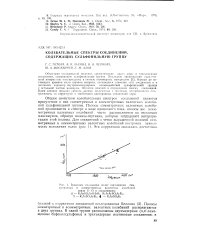
График зависимости между а и IgA.| Коэффициенты корреляции зависимости vcN2 - з. [10] |
Интересно отметить, что в ряду диазосоединений столь же большой интенсивностью обладает диазогруппа в n - хинондиазидах ( табл. 3), в то время как интегральная интенсивность Асыг о-хинондиазидов относительно невелика ( 5 3 - 5 5 практ. Нужно думать, что величина интегральной интенсивности группы CN2 характеризует силу внутримолекулярных взаимодействий диазоние-вой группы с ароматической системой: в катионе и-нитрофенилдиазо. К-диметиламинофенилдиазония, имеющий высокое значение интегральной интенсивности Асн2, обладает, по-видимому, и сильными внутримолекулярными взаимодействиями. [11]
 |
Взаимное положение полос поглощения симметричных и асимметричных валентных колебаний. [12] |
Объектами исследований являлись ароматические одно -, двух - и трехъядерпые соедниения, содержащие сульфонильную группу. Однако до настоящего времени мало изучены вопросы, касающиеся строения УТИХ соединений и в-частпости характер внутримолекулярных взаимодействий сульфонилыюй группы с остальной частью молекулы. Остается неясной и стереохимия многих соединений. Нами сделана попытка связать данные, полученные с помощью абсорбционной спектроскопии, со структурой п свойствами кислородных соединений серы. [13]
 |
Взаимодействие оптически активного краун-эфира ( S - 201 и нециклического полиэфирного гомолога (. - 202с солями эфиров / аминокислот [ / - RCH ( NH CO-Ar ]. [14] |
Для солей / - аминоэфиров, имеющих первичные ионы аммония, как, например, соли глицинового, аланинового и валинового эфиров, наоборот, скорость реакции с циклическим полиэфиром, имеющим SH-группы, была примерно в 100 раз выше скорости реакции с нециклическим аналогом, а для фенилаланина и лейцина - соответственно в 500 и 1000 раз выше. Эти результаты отражают более упорядоченную структуру комплексов циклических краун-эфиров по сравнению с нециклическими. Так же как скорость реакции может быть увеличена за счет внутримолекулярного взаимодействия групп, так и изменение межмолекулярной конфигурации при комплексообразовании может влиять на скорость реакции. [15]
Страницы: 1 2