Идеальность
Cтраница 3
Отклонения от идеальности определяются разностью величин ( dpldT) y двух веществ. Степень отклонения пропорциональна величине Т ( др. дТ) у. Эта величина примерно равна внутреннему давлению. Следовательно, раствор ведет себя как идеальный только в том случае, если внутренние давления компонентов равны. Так как внутреннее давление определяется силами молекулярного притяжения и отталкивания, то причиной отклонения реальных растворов от идеальности является различие в силах взаимодействия между молекулами в растворе. [31]
Отклонения от идеальности при этом уменьшаются, но остаются отрицательными. [32]
Отклонения от идеальности проявляются при растворении в этом растворителе полярных веществ, таких, как хлороформ и крезолы. Значительно большие отклонения характерны для растворов карбоновых кислот алифатического и ароматического рядов. [33]
Отклонения от идеальности невелики; при более высоких давлениях они могут значительно возрасти. [34]
Отклонение от идеальности объясняется главным образом различием силовых полей разноименных молекул. [35]
Если же идеальность имеет место только при хг - 0 то ( 22 5 8) является законом Генри. [36]
Отклонения от идеальности в жидкой фазе удобно представить в виде факторов-сомножителей. [38]
Отклонение от идеальности является, таким образом, результатом влияния энтропийного члена. Для системы бензол - динонилфталат величины & e - f и Т & esf почти идентичны. [39]
Отклонение от идеальности является, таким образом, результатом влияния энтропийного члена. Для системы бензол - динонилфталат величины Agpf и Т Де 5 почти идентичны. [40]
Отклонения от идеальности в реальных растворах особенно велики у сильных электролитов. Это обусловлено тем, что электрические силы ионов проявляются на более значительных расстояниях, чем молекулярные силы, действующие между молекулами газа. Энергия взаимного притяжения между молекулами убывает пропорционально шестой степени расстояния между ними. Энергия взаимного притяжения между ионами убывает пропорционально первой степени расстояния между ними. Поэтому при повышении концентрации раствора, когда частицы растворенного вещества сближаются, силы ионного взаимодействия начинают сказываться много раньше и много сильней, чем силы молекулярного притяжения. [41]
Отклонения от идеальности в подвижной фазе приводят к тому, что коэффициенты активности, вычисленные по упругости пара, более чувствительны к температуре, чем вычисленные по фугитив-ности. [42]
 |
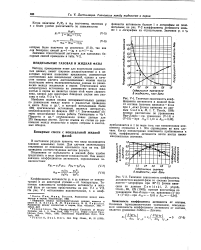
Зависимость коэффициента фугитивности паровой фазы от. [43] |
Отклонения от идеальности невелики; при более высоких давлениях они могут значительно возрасти. [44]
 |
Идеальная тепловая машина Карно. [45] |
Страницы: 1 2 3 4