Идея - льюис
Cтраница 1
Идея Льюиса в дальнейшем была использована при разработке теории ковалентной связи. [1]
Используя упомянутую идею Льюиса, мы будем считать, что любая нормальная связь между двумя атомами должна осуществляться с помощью двух электронов. [2]
Согласно идее Льюиса, давление и концентрация в уравнениях состояния и химического потенциала для идеального случая заменяются новыми величинами, подстановка которых в эти уравнения делает их пригодными для реального состояния. Эти величины связаны с давлением и концентрацией не прямо пропорциональной зависимостью. [3]
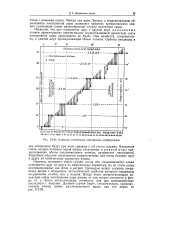 |
П-34. Наиболее устойчивые электронные конфигурации. [4] |
Между тем идея Льюиса о первоначальном образовании электронной пары позволяет охватить принципиально единой трактовкой самые разнообразные случаи валентной связи. [5]
Сиджвик принял идеи Льюиса о двухэлектронной ковалент-ной связи между двумя атомами в молекуле и ввел понятие координационной связи для случая, когда оба электрона, образующие связь, поставляются одним атомом. Заметив, что все молекулы или ионы, которые могут присоединяться к иону металла, имеют по крайней мере одну неподеленную пару электронов, он предположил, что эта свободная электронная пара частично может быть отдана иону металла при образовании связи. Такую связь называют дативной или семиполярной и иногда изображают стрелкой ( М - L), которая указывает, что донорная группа ( L) поставляет на связь с акцептором ( М) оба электрона. [6]
Сиджвик принял идеи Льюиса о двухэлектронной ковалентной связи между двумя атомами в молекуле и ввел понятие координационной связи для случая, когда оба электрона, образующие связь, поставляются одним атомом. Заметив, что все молекулы или ионы, которые могут присоединяться к иону металла, имеют по крайней мере одну неподеленную пару электронов, он предположил, что эта свободная электронная пара частично может быть отдана иону металла при образовании связи. Такую связь называют дативной или семиполярной и иногда изображают стрелкой ( M - - L), которая указывает, что донорная группа ( L) поставляет на связь с акцептором ( М) оба электрона. [7]
На основе идеи Льюиса была разработана теория химической связи, получившая название метода валентных связей ( метод ВО. Теория охватывала все молекулы, простые и сложные, а также и твердые вещества. [8]
Фактически сразу же было замечено, что гипотеза обменного вырождения эквивалентна старой электронной идее Льюиса, согласно которой химическая связь образуется спариванием электронов с противоположными спинами. Электронная пара в свою очередь представляет собой интерпретацию традиционного валентного штриха в химических формулах. [9]
Укажем, наконец, что вышеизложенная интерпретация структурной теории ( в трактовке Льюиса) не является единственно возможной, так как сам перевод идеи Льюиса на язык квантовой механики не вполне однозначен. [10]
В предыдущем разделе была обсуждена теория метода валентных связей ( ВС), или метода электронных пар. Основа этой теории - идея Льюиса о том, что каждая пара атомов в молекуле удерживается вместе при помощи электронной пары или, возможно, нескольких электронных пар. Эти пары электронов локализованы между определенными парами ядер. [11]
Но его последователь Лангмюр в многочисленных статьях популяризировал идеи Льюиса, присоединив к ним несколько своих оригинальных положений. [12]
Основное достоинство представлений Косселя заключается в простоте и наглядности, основной недостаток - в их ограниченной применимости. Действительно, все органические соединения и очень многие неорганические построены по неионному типу и поэтому не могут рассматриваться с ионной точки зрения без сильного расхождения результатов с данными опыта. Между тем идея Льюиса о первоначальном образовании электронной пары позволяет охватить принципиально единой трактовкой самые разнообразные случаи валентной связи. [13]
Основное достоинство представлений Косселя заключается в простоте и наглядности, основной недостаток - в их ограниченной применимости. Действительно, все органические соединения и очень многие неорганические построены по неионному типу и поэтому не могут рассматриваться с ионной точки зрения. Между тем идея Льюиса о первоначальном образовании электронной пары позволяет охватить принципиально единой трактовкой самые разнообразные случаи валентной связи. [14]
В 1927 г. Льюис выдвинул гипотезу, что энтропия стремится к нулю, когда при неизменной температуре бесконечно повышается давление. Это утверждение как бы является аналогом закона Нернста, по которому энтропия стремится к нулю, когда при неизменном давлении бесконечно повышается величина 1 / Т, где Т - абсолютная температура. Мне кажется, что эта идея Льюиса не имеет и тени правдоподобия. [15]
Страницы: 1 2