Избыток - окись - углерод
Cтраница 1
Избыток окиси углерода не оказывает вредного влияния на синтез, одновременно подавляя реакцию метанообразования; для сохранения выходов продуктов необходимо несколько повысить температуру синтеза. [1]
Избыток окиси углерода недопустим, так как он благоприятствует реакциям полимеризации. [2]
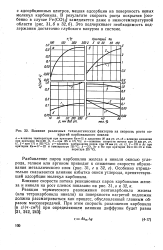 |
Влияние различных технологических факторов на скорость роста покрытий карбонильного никеля. [3] |
Особенно отрицательно сказывается влияние избытка окиси углерода, препятствующей адсорбции молекул карбонила. [4]
Пламя при неполном горении содержит избыток несгоревшей окиси углерода и водород. Окись углерода и водород при температурах ниже 1000 С обладают свойством жадно соединяться с кислородом. Отнимая от окисленной поверхности железа кислород, они могут даже восстанавливать железо из окалины. В печи с пламенем, содержащим большое количество окиси углерода и водород, образования окалины не происходит. Такое пламя называется восстановительным. Если горение топлива протекает полно, при нормальной подаче воздуха, то в продуктах горения не будет излишков кислорода, а пламя, полученное три таком режиме, называется нейтральным. [5]
Было найдено, что в богатых смесях, содержащих избыток окиси углерода, результаты измерения температуры обеими проволоками не очень сильно отличаются друг от друга. В бедных же смесях, содержащих избыток кислорода, проволочка, покрытая кварцем, давала гораздо более низкую температуру. Полученные этими авторами кривые приведены на фиг. Здесь Тр и Tq представляют собой температуры, измеряемые соответственно оголенным и покрытым кварцем платинородиевыми термометрами. [6]
После охлаждения бомбы до комнатной температуры из нее выпускают избыток окиси углерода. [7]
Железные катализаторы в отличие от кобальтовых вследствие того, что синтез над ними протекает при более высоких температурах, легко подвержены при этом окислению кислородом воды в случае отсутствия в газе избытка окиси углерода. При наличии в газе избыточных количеств окиси углерода окисления катализатора не происходит, так как образующаяся вода реагирует с окисью углерода с образованием углекислоты и водорода. Скорость реакции конверсии при температурах синтеза значительно выше скорости окисления, поэтому высокая концентрация окиси углерода в синтез-газе и способность катализатора ускорить конверсию окиси углерода водой предохраняет катализатор от окисления и снижения его активности. [8]
Недавно был выработан совершенно новый метод [47] получения фторуксусной кислоты из фтористого водорода, окиси углерода и формальдегида. Избыток окиси углерода прибавляют к двум другим компонентам, взятым в молярных соотношениях. [9]
Такой ход реакций принято называть косвенным восстановлением. Оно протекает при умеренных температурах ( примерно в интервале от 300 до 950) и требует, как это видно из вышеприведенных уравнений, избытка окиси углерода. Это объясняется тем, что один из продуктов восстановления - углекислота - может окислять РеО до Fe3O4 и Fe до FeO, если концентрация СО2 в газах превышает определенные пределы, зависящие от температуры. [10]
В связи с этим Уатсон114 недавно показал, что распад этот точно так же, как и разложение этоксиоксало-пропионового эфира и этоксиоксалосукционового эфира, в температурном интервале между 140 и 200 следует мономолеку-яярному закону. На ход реакции не оказывают влияния такие растворители, как бромнафталин и неролин или газообразный хлористый водород или влага. Избыток окиси углерода, напротив, замедляет ее. Оказывается, что константа скорости меняется в зависимости от температуры, согласно закону Аррениуса, k - Ae - jKT, и если А представляет собой возможность распада115 активной молекулы в секунду, то надо ожидать существования зависимости для родственных соединений, и Ватсон обнаружил, что Q / logA - величина постоянная. [11]
Более сильное влияние оказывает присутствие в синтез-газе соединений, которые могут участвовать в реакции. Одним из таких соединений является, естественно, вода, подавляющая образование высших спиртов. Поэтому избыток окиси углерода, конверсия которой с образованием двуокиси приводит к удалению воды, в весьма сильной степени благоприятствует протеканию реакции. [12]
 |
Синдром вредных зданий. [13] |
На рис. 13.1 перечислены симптомы, обычно включаемые в понятие SBS. В последние годы с учетом накапливающихся данных из списка обычно исключались жалобы, связанные с запахами, а симптоматика со стороны органов дыхания была переведена в разряд симптомов раздражения слизистых оболочек. Необходимо проведение тщательной дифференциальной диагностики между SBS и заболеванием, связанным со зданием ( BRI), для которого характерны клинические проявления в виде реакций раздражения, аллергии, или таких заболеваний как пневмония, обусловленная гиперчувствительностью, астма и приступы головных болей, вызванные присутствием в воздухе избытка окиси углерода. Необходимо также отличать SBS от множественной чувствительности к химическим агентам ( MCS, см. далее), которая встречается реже, часто отмечается у лиц, страдающих SBS, и гораздо слабее реагирует на мероприятия по улучшению среды в рабочих помещениях. [14]
Окись углерода и водород сначала адсорбируются на поверхности катализатора. Затем окись углерода подвергается хемосорбции на активных центрах катализатора [112] с ослаблением углерод-кислородной связи. Водород или избыток окиси углерода на железе реагируют с кислородом, образуя соответственно воду или углекислоту. При дальнейшем действии водорода карбидный углерод превращается в радикалы СН, СН2 и СН3, которые полимеризуются затем в разнообразные углеводороды. По мере удлинения углеводородной цепи десорбция продуктов реакции с каталитической поверхности все более и более замедляется, и, таким образом, увеличивается период времени, необходимый для полного гидрирования водородом. На основании предположения, высказанного Фишером и Кохом, можно было легко объяснить постоянное падение ненасыщенности продуктов реакции по мере возрастания температуры кипения. В некоторых условиях высокомолекулярные углеводороды, подвергаясь крекингу, могут расщепляться на более мелкие части; таким образом, устанавливается равновесие между процессами полимеризации и крекинга. [15]
Страницы: 1 2