Избыток - электронная плотность
Cтраница 1
Избыток электронной плотности с т, -; называется положительной спиновой плотностью. Положительная спиновая плотность изображается стрелкой, направленной вдоль внешнего поля, а отрицательная плотность изображается стрелкой, направленной против поля. [1]
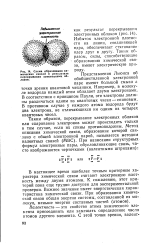 |
Схема образования химических связей в результате перекрывания электронных облаков. [2] |
Избыток электронной плотности на линии, соединяющей ядра, обеспечивает стягивание ядер друг к другу. Таким образом, силы, способствующие образованию химической связи, имеют электрическую природу. [3]
Действительно, в молекуле имеется избыток электронной плотности в орто-и пара-положениях, и электрофилы атакуют преимущественно эти центры. [4]
Знак ( -) здесь и далее означает избыток электронной плотности, знак () - недостаток электронной плотности. Знаками - и t без скобок обозначаются заряды ионов. [5]
Знак ( -) здесь и далее означает избыток электронной плотности, знак () - недостаток электронной плотности. Знаками - и без скобок обозначаются заряды ионов. [6]
Знак ( -) здесь и далее означает избыток электронной плотности, знак) - недостаток электронной плотности. Знаками - и без скобок обозначаются заряды ионов. [7]
Знаками 8 и 6 - показаны дефицит и избыток электронной плотности на участке СС-связи в пропене. Метальная группа смещает электронную плотность по ст-связи к СН-группе. [8]
Знаками 5 и 5 - показаны дефицит и избыток электронной плотности на участке С С-связи в пропене. Метильная группа смещает электронную плотность по а-связи к СН-группе. [9]
Знак ( -) здесь и далее означает избыток электронной плотности, знак () - недостаток электронной плотности. [10]
 |
Шкала электроотрицательности элементов. [11] |
Частичные заряды б и б - выражают дефицит или избыток электронной плотности. Это различие в электронной плотности является следствием большей электрофильности атомов кислорода и хлора по сравнению с атомами фосфора или углерода. Какой из атомов несет частичный отрицательный заряд 6 -, а который - положительный 6, можно оценить исходя из электроотрицательности того или иного элемента. [12]
При сдвиге электронных облаков, обозначенном в схеме стрелками, наи-больший избыток электронной плотности ( обозначаемый б -) будет у атомов углерода в орто - и пара-положении по отношению к заместителю. Поэтому при общем повышении подвижности атомов водорода наиболее легко эти атомы замещаются в орто-к пара-положении. В настоящее время доказано, что при действии на фенол дейтерио-кислот, например D2S04, атомы водорода в орто - и пара-положении легко замещаются дейтерием. Механизм реакций замещения в бензольном кольце в настоящее время трактуется в большинстве случаев как процесс замещения наиболее подвижных атомов водорода катионами или катионоидными радикалами. [13]
При сдвиге электронных облаков ( обозначенном в схеме стрелками) наибольший избыток электронной плотности ( обозначаемый 6 -) будет у атомов углерода в орто и пара-положении по отношению к заместителю. Поэтому при общем повышении подвижности атомов водорода наиболее легко эти атомы замещаются в орто - и пара-положении. [14]
Возможен и другой механизм - присоединение к дегидро-бензолу фенокси-аниона, в о-положении которого имеется избыток электронной плотности. [15]
Страницы: 1 2 3 4