Избыток - хлорангидрид
Cтраница 1
Избыток хлорангидрида [2108, 3404] или добавление в реакционную массу пятихлористого фосфора [3406] способствует образованию трифенилхлорсилана. [1]
Когда избыток хлорангидрида оптически чистой ( Д) - О-метил-миндальной кислоты реагирует с образцом частично расщепленного 1-фенилэтиламина, [ а ] и 22 6 ( с 8 6, метанол), образуются только два из четырех возможных диастереомеров, а именно 1е и 1з, и отношение диастереомеров 1е / 1з равно отношению энантиомеров 1б / 1а в исходном 1-фенилэтиламине. [2]
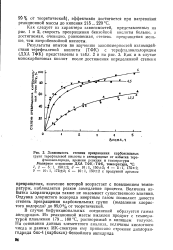 |
Зависимость степени превращения карбоксильных групп терефталевой кислоты в ангидридные от избытка тере. [3] |
Величина избытка хлорангидрида также не оказывает существенного влияния. Отдувка хлористого водорода инертным газом позволяет довести степень превращения карбоксильных групп ( выделение хлористого водорода) до 99 0 % от теоретической. [4]
После охлаждения избыток хлорангидрида эте-рифицируют с помощью 27 мл метанола. [5]
Для удаления избытка хлорангидрида энантовой кислоты смесь перемешивают с диэтиламиноэта-нолом и выливают в раствор разбавленной соляной кислоты. Чистоту препарата определяют по отсутствию сульфатной золы и энантовой кислоты. [6]
Нами ДМАГХ получен взаимодействием избытка хлорангидрида метакриловой кислоты с гидрохиноном ( 0 75 мол. [7]
Обычно для получения кетонов в избыток хлорангидрида в эфирном растворе вводят при охлаждении реактив Гриньяра. Нагревание снижает выход кетона за счет побочных реакций. [8]
При проведении последующих опытов употребляли избыток хлорангидрида трифторуксусной кислоты, вместо избытка гидрида, так как последний трудно доступен; таким образом, было использовано 95 / 0 гидрида, однако такая методика работы не может быть рекомендована. [9]
Показано, что для синтеза диметакрилата гидрохинона взаимодействием хлорангидрида метакриловой кислоты с гидрохиноном необходим избыток хлорангидрида. При проведении синтеза диметакрилата пирокатехина в условиях, аналогичных условиям синтеза диметакрилата гидрохинона, образуется монометакрилат пирокатехина. [10]
Реакционную смесь оставляют в покое на два дни при комнатной температуре, затем ставят в лед, разлагают избыток хлорангидрида кислоты небольшим количеством воды, извлекают 300 мл уфира и выщелачивают последовательно холодным насыщенным раствором бисульфата калия и раствором бикарбоната натрия. После высушивания сульфатом натрия отгоняют эфир в вакууме при комнатной температуре, растноряют оставшийся сироп примерно в IVa частях хлороформа и добавляют 7 объемных частей петролейного эфира. [11]
В этих случаях процесс проводят при низкой температуре ( 0 С), постепенно добавляя при перемешивании спирт или фенол к избытку хлорангидрида. [12]
Применение хлористого алюминия в хлор-ангидридах кислот ( например, хлористом тиониле или хлористом бензоиле) способствует циклизации при очень низких температурах, и в присутствии избытка хлорангидрида кислоты отщепления ацил-аминогрупп не происходит. Для циклизации антримидов с ацил-аминогруппами в молекуле применяется также молекулярное соединение хлористого алюминия и ароматического нитрила. Антрахи-нонкарбазоловые красители, образующиеся обычно при циклизации, сопровождающейся потерей атома водорода и образованием С-С связи, могут быть синтезированы и другими методами. [13]
Поскольку после дегидратации амида, очевидно, должен происходить гидролиз избытка хлорангидрида кислоты, следует вводить стехиомет-рическую поправку на содержание в смеси спиртов или аминов. Есть основание полагать, что оба эти типа соединений количественно реагируют с хлористым 3 5-динитробензоилом. [14]
 |
ИК-спектр поглощения. [15] |
Страницы: 1 2 3