Извлечение - ниобий
Cтраница 3
 |
Распространение хлорирования в брикетированном слое. [31] |
Уже при 450 С достигается высокое извлечение ниобия ( более 95 %), в то время как вскрытие циркона незначительно. [32]
Установлена зависимость между растворимостью циклогексанона в водном растворе после экстрагирования и степенью извлечения ниобия. Чем больше растворимость экстрагента, тем меньше степень извлечения ниобия циклогексано Ном. Для некоторых опытов нагревание раствора приводит к увеличению извлечения ниобия. [33]
Комплексообразовапие титана с ниобием и танталом может использоваться в качестве метода для переведения последних в раствор. Неустойчивость образующихся комплексов в разбавленных водных растворах может использоваться для извлечения ниобия и тантала из растворов методом гидролиза при нагревании. [34]
Если процесс проводят в шахтной электропечи, то концентрат и углеродсодержащий восстановитель ( древесный уголь, нефтяной кокс и др.) брикетируют. В качестве связующего применяют сульфит-целлюлозный щелок ( отход бумажного производства), пек, кормовую патоку и др. Углерод берут с избытком 7 - 10 %, так как меньшее содержание углерода снижает извлечение ниобия, тантала и титана. Повышенное содержание в шихте углерода не увеличивает извлечение ценных составляющих, но снижает загрузку по концентрату. Брикеты сушат, а затем нагревают без доступа воздуха при 800 - 900 С. При этом полностью удаляются влага и летучие компоненты шихты. На брикеты действуют газообразным хлором при 600 - 900 С. Хлор должен содержать минимальное количество влаги, чтобы не было гидролиза продуктов хлорирования. [35]
Механизм экстракции ниобия из фторидных растворов изучен мало. Эти выводы сделаны на основании данных химического анализа экстрактов. На возможность извлечения ниобия в виде HNbOF4 и H2NbF7 указывается и в других работах [257, 297, 1105], но высказанные предположения не подтверждены экспериментальными данными. [36]
Наиболее полное использование ниобия достигается npv восстановлении его алюминием. Этот метод широко применяют в промышленности. Максимально возможный уровеш извлечения ниобия из Nb2Os при протекании алюминотер-мического восстановления по реакции 3Nb2O5 10Al 61 тЬ 5А12Оз определяется равновесными концентрациями ниобия в сплаве и оксида Nb2Os в шлаке. Высокотемпературное восстановление Nb2O; алюминием протекает в диффузионном режиме и лимитирующей стадией процесса является подвод ионов ниобия из оксидного расплава к границе раздела металлической и шлаковой фаз, поэтому повышение температуры расплава вызывает снижение концентрации МЬ2Об в шлаковом расплаве. [37]
Наиболее полное использование ниобия достигается при восстановлении его алюминием. Этот метод широко применяют в промышленности. Максимально возможный уровень извлечения ниобия из Nb2Os при протекании алюминотер-мического восстановления по реакции 3Nb2O5 10Al 61 тЬ - - 5А12Оз определяется равновесными концентрациями ниобия в сплаве и оксида Nb2Os в шлаке. Высокотемпературное восстановление Nb2Os алюминием протекает в диффузионном режиме и лимитирующей стадией процесса является подвод ионов ниобия из оксидного расплава к границе раздела металлической и шлаковой фаз, поэтому повышение температуры расплава вызывает снижение концентрации Nb2O5 в шлаковом расплаве. [38]
Экстракция ниобия зависит и от природы органического растворителя. Так, в случае ТБФ [1140, 1143], изо амилацетата [1151], ацетофенона, бензальдегида [1153], диизопропилкетона [ 11561 ниобий практически не извлекается в органическую фазу при низких и умеренных концентрациях НС1 ( 3 - 7 М), но при дальнейшем увеличении CHCI извлечение резко возрастает и уже при CHCI 8 - 9 М приближается к полному. Следует подчеркнуть плохую воспроизводимость данных о полноте извлечения ниобия. Например, Гибало и Альбадри [1146], в отличие от Кольцова и Коровина [257] - а также Старцева и Крылова [1143], нашли, что ТБФ начинает заметно извлекать ниобий уже при CHCI 1 - 2 М, а на кривой зависимости степени извлечения от CHCI нет резкого скачка. Противоречивы данные и о максимальной степени извлечения. [39]
Установлена зависимость между растворимостью циклогексанона в водном растворе после экстрагирования и степенью извлечения ниобия. Чем больше растворимость экстрагента, тем меньше степень извлечения ниобия циклогексано Ном. Для некоторых опытов нагревание раствора приводит к увеличению извлечения ниобия. [40]
 |
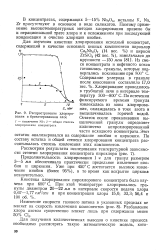
Зависимость степени извлечения ниобия в растворы фтористоводородной кислоты от иродолжи-тельности выщелачивания концентрата. [41] |
Из анализа кривых видно, что наиболее интенсивный переход ниобия в раствор наблюдается в течение первого часа обработки. При выщелачивании 15 % - м раствором фтористоводородной кислоты в течение 1 часа в раствор переходит 95.0 % Nb205, а при выщелачивании 20 % - и HF такое же количество ниобия переходит в раствор за 30 минут. Дальнейшее увеличение продолжительности выщелачивания свыше 1 часа незначительно сказывается на извлечении ниобия. [42]
Для извлечения растворимой части элементов из промывных растворов могут быть применены как сильноосновные, так и слабоосновные аниониты. К числу недостатков сильноосновного анионита АВ-17X8 следует отнести медленное вымывание из него тантала. Этим недостатком не обладают слабоосновные аниониты, при использовании которых процесс извлечения ниобия и тантала может быть осуществлен на одной колонке. [43]
Недавно был найден еще один источник ниобиевого сырья, которое оказалось особенно выгодным для извлечения ниобия, - месторождения пирохлора. Он представляет собой, по существу, смешанный кальциево-натрие-вый ниобат, содержащий некоторое количество фторидов, а часто и заметные количества титана и церия. Особенно ценно то, что некоторые образцы пирохлора почти не содержат тантала, и поэтому их можно сразу направлять на извлечение ниобия. [44]
Нами установлено, что при экстракции протактиния с БФГА из растворов 3 5 М серной кислоты протактиний извлекается полностью в присутствии больших количеств алюминия, железа, тория, урана, висмута, олова, титана ( III), редкоземельных элементов и др. Перечисленные элементы не экстрагируются в этих условиях. В присутствии весовых количеств Mo ( VI), Nb, V ( V), Ti ( IV) и Sb ( III) экстракция протактиния сильно ухудшается. Применение щавелевой кислоты в этом случае также полезно для ослабления влияния этих элементов на экстракцию протактиния и подавления извлечения ниобия и циркония. Следует отметить, что вводимые количества щавелевой кислоты должны быть близки по стехиометрии к содержанию циркония и ниобия, так как большой избыток Н2С204 снижает экстракцию протактиния. Причем снижение степени извлечения протактиния находится в линейной зависимости от концентрации щавелевой кислоты. Как оказалось, после введения щавелевой кислоты в растворы, содержащие цирконий, в процессе встряхивания в водной фазе выпадает осадок. В состав этого осадка, кроме БФГА и циркония, по-видимому, входит и щавелевая кислота. [45]
Страницы: 1 2 3 4