S-образный вид
Cтраница 3
При скоростной седиментации или при свободной или дифференциальной диффузии кривые распределения концентрации имеют S-образный вид. Но так как оптические схемы дают обычно колоколообразные кривые градиента концентрации ( или такие кривые можно получить дифференцированием по координате или времени), то и в этом случае алгоритмика не изменяется: замена самой концентрации на ее производную практически никакого значения при обратном преобразовании не имеет. [31]
Кривая изменения удельной поверхности материала при диспергировании ( см. рис. 2) имеет специфический S-образный вид. В самом начале размола удельная поверхность растет мало, затем до 20 час резко увеличивается до 400 м2 / г, причем максимум скорости роста лежит между 5 и 10 час. [32]
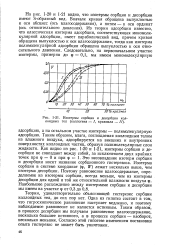 |
Изотермы сорбции и десорбции коллоидных тел ( коллогена - /, крахмала - / /. [33] |
На рис. 1 - 20 и 1 - 21 видно, что изотермы сорбции и десорбции имеют S-образный вид. Из теории адсорбции известно, что классическая изотерма адсорбции, соответствующая мономолекулярной адсорбции, имеет параболический вид, причем кривая обращена выпуклостью к оси влагосодержания, тогда как изотерма полимолекулярной адсорбции обращена выпуклостью к оси относительного давления. [34]
Кинетические кривые радиационной полимеризации ТФХЭ в массе при мощности дозы от 1 до 400 рд / сек имеют характерный S-образный вид. До 10 - 15 % конверсии наблюдается линейная зависимость конверсии от времени облучения. Затем наблюдается уменьшение скорости полимеризации. [35]
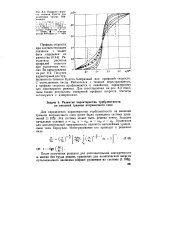 |
Профили скорости течения Куэтта при различных числах Рей-нольдса. [36] |
Результаты расчетов профилей скорости при различных числах Re представлены на рис. 8.2. Получен характерный для турбулентного течения Куэтта S-образный вид профилей скорости. С уменьшением числа Рейнольдса г течение перестраивается, а профили скорости приближаются к линейному, характерному для ламинарного режима. Для сопоставления на рис. 8.2 показаны также результаты измерений профиля скорости. Расчеты согласуются с измерениями. [37]
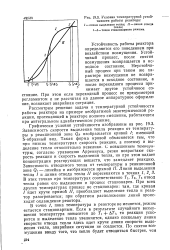 |
Условия температурной устойчивости работы реактора. [38] |
Графически условия устойчивости изображены на рис. 19.3. Зависимость скорости выделения тепла реакции от температуры в реакционной зоне Qr изображается кривой /; имеющей S-образный вид. Такая форма кривой объясняется тем, что при низких температурах скорость реакции, а поэтому и выделение тепла относительно невелики. С повышением температуры, согласно уравнению Аррениуса, резко возрастают скорость реакции и скорость выделения тепла, но при этом падает концентрация реагирующих веществ, что замедляет реакцию. В этих точках при температурах соответственно 7Ь Т2, Тг отвод тепла равен его выделению и процесс стационарен. При всех других температурах процесс не стационарен: там, где кривая / идет круче прямой / /, преобладает выделение тепла и реактор разогревается; при обратном расположении линий происходит охлаждение реактора. [39]
 |
Условия температурной устойчивости работы реактора. [40] |
Графически условия устойчивости изображены на рис. 19.3. Зависимость скорости выделения тепла реакции от температуры в реакционной зоне QR изображается кривой /; имеющей S-образный вид. Такая форма кривой объясняется тем, что при низких температурах скорость реакции, а поэтому и выделение тепла относительно невелики. С повышением температуры, согласно уравнению Аррениуса, резко возрастают скорость реакции и скорость выделения тепла, но при этом падает концентрация реагирующих веществ, что замедляет реакцию. В этих точках при температурах соответственно Т, Т %, Т3 отвод тепла равен его выделению и процесс стационарен. При всех других температурах процесс не стационарен: там, где кривая / идет круче прямой / /, преобладает выделение тепла и реактор разогревается; при обратном расположении линий происходит охлаждение реактора. [41]
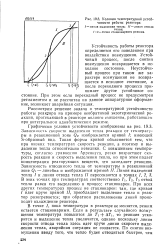 |
Условия температурной устойчивости работы реактора. [42] |
Графически условия устойчивости изображены на рис. 19.3. Зависимость скорости выделения тепла реакции от температуры в реакционной зоне QK изображается кривой /; имеющей S-образный вид. Такая форма кривой объясняется тем, что при низких температурах скорость реакции, а поэтому и выделение тепла относительно невелики. С повышением температуры, согласно уравнению Аррениуса, резко возрастают скорость реакции и скорость выделения тепла, но при этом падает концентрация реагирующих веществ, что замедляет реакцию. В этих точках при температурах соответственно Т, Т2, 7 з отвод тепла равен его выделению и процесс стационарен. При всех других температурах процесс не стационарен: там, где кривая / идет круче прямой / /, преобладает выделение тепла и реактор разогревается; при обратном расположении линий происходит охлаждение реактора. [43]
Они показали, что при переходе от сульфатного к кислому иодидному раствору ( серная кислота с добавкой иодида калия) изотерма адсорбции катиона децилпиридиния приобретает S-образный вид, причем отталкивание в адсорбционном слое сменяется сильным притягательным взаимодействием. Это обусловлено тем, что в присутствии иодида калия адсорбция органического катиона идет по слою специфически адсорбированных анионов и сопровождается сильным притягательным взаимодействием между разноименно заряженными частицами. [44]
В работе 51 приведены кривые ползучести феноло-формальде-гидной смолы по данным Лидермана, из которых видно, что в интервале температур 90 - 100 С кривая имеет S-образный вид, характерный для систем, полученных введением пластификатора в полярный линейный полимер. В области 100 - 120 С эти кривые вырождаются в обычные кривые ползучести с ясно выраженным участком высокоэластических деформаций. [45]
Страницы: 1 2 3 4