Свободная анергия
Cтраница 2
Термодинамическая невыгодность контактов между неполярными частями больших молекул и водой определяется повышением свободной анергии. Небольшие неполярные молекулы ( СН4, С2Н и др.) при очень малых концентрациях могут растворяться в воде, размещаясь в пустых промежутках между большими ассоци-атами молекул воды. Свободная энергия при этом понижается за счет вандерваальсовых взаимодействий и повышения энтропии смешения. Такая растворимость, однако, реэко снижается при увеличении размеров молекул. [16]
Поверхностным натяжением ч называется работа, необходимая для образований еде - u noiepxnocTi, или свободная анергия единицы поверхности. [17]
Наибольший интерес в настоящее время представляет предложенное Ю. В. Танчуком [45] выражение ГЛБ, которое можно получить с использованием принципа линейности свободных анергий. Величина KKMj и стандартное мольное уменьшение свободной энергии ассоциации ПАВ в растворе связаны соотношением - & Fuass HT In ККМ. [18]
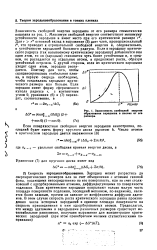 |
Зависимость свободной энергии образования зародыша в пленке от его размера. [19] |
Для г г основной вклад в выражение ( 3) дает член, пропорциональный Is, что приводит к отрицательной свободной анергии и, следовательно, к устойчивости зародышей большого радиуса. Если к зародышу критического радиуса ( так называемому критическому зародышу) добавляется еще один атом, то он ( зародыш) становится чуть более устойчивым и, в среднем, не распадается на отдельные атомы, а продолжает расти, образуя устойчивый островок. С другой стороны, если из критического зародыша уходит один атом, зародыш распадается. Поэтому для того, чтобы сконденсировалась стабильная пленка, в первую очередь необходимо, чтобы создавались зародыши критического размера или больше. [20]
При этом сплав переходит в более стабильное состояние, хотя обычно и далекое от истинного равновесия, для которого характерен абсолютный минимум свободной анергии. Процессы распада пересыщенного раствора IB закаленном сплаве, так же как возврат и рекристаллизация, протекают самопроизвольно, с выделением тепла. [21]
Механохимическое промотирование катализаторов при их диспергировании основано на том, что при диспергировании - вновь раскрываются пов-ерхности катализатора, наиболее неравновесные с точки зрения избытка свободной анергии, еще не дезактивированные контактом с внешней средой. Это направление весьма перспективно в области гетерогенного катализа. [22]
Увеличение скорости кристаллизации и числа центров при малых степенях переохлаждения обусловлено тем, что вблизи точки ts подвижность жидкости велика и ускорение кристаллизации вызывается увеличением разности свободных анергий жидкого и кристаллического состояний. Наоборот, снижение скорости кристаллизации и числа центров при больших степенях переохлаждения вызвано тем, что подвижность атомов небольшая, следовательно, уменьшена и способность системы к превращению, так как разность свободных энергий жидкого и кристаллического состояний мала. [23]
Поскольку свободная анергия, G, подобно функциям Я, Т и S, которые в нее входят, представляет собой функцию состояния, не имеет значения, изменяются ли в ходе реакции. [24]
В литературе энергия Гиббса также называется свободной энергией. Иногда термин свободная анергия употребляется для представления функции Гельмгольца, называемой также максимальной полезной работой. Некоторые авторы энергию Гиббса обозначают символом F. В этой книге все рассуждения о свободной энергии относятся к функции Гиббса О. [25]
Верхний индекс ( ф) используется для указания на то, что речь идет о процессе, связанном с переходным состоянием или активированным комплексом. Эта свободная энергия называется свободной анергией активации. [26]
Предложено несколько теорий для объяснения возможности роста монокристаллов со сложенными цепями из разб. Большинство из них базируется на расчетах свободной анергии. При атом постулируется, что тепловые колебания в кристалле вызывают уменьшение энергии взаимодействия ( увеличение амплитуды колебаний) между соседними цепями, к-рое тем значительнее, чем длиннее цепь. [27]
На основании второго закона термодинамики самопроизвольные процессы идут в направлении перехода энергии от тел с более высоким потенциалом ее к телам с более низким потенциалом; при этом часть свободной энергии системы превращается в полезную работу. Отсюда следует вывод, что самопроизвольно идущие процессы сопровождаются уменьшением свободной анергии системы. [28]
Как известно из термодинамики, константа равновесия связана со свободной энергией процесса. Эту связь можно использовать и для нахождения величины К, вводя понятие свободная анергия активации, характеризующее изменение свободной энергии при переходе системы из исходного состояния в переходное и учитывающее все степени свободы, кроме координаты реакции. [29]
То есть при оувественном различия ( в четыре раза) в величинах Дй и примерном равенстве избыточных энергий смешения для обеих систем ваблядавтея одинаковые во абсолютно величине нвбыточные сдвиг. Таким образом, данные для рассмот-ревных систем бензол - ацетон и бензол - гексан подтверждав сделанное ранее предположение о сущвствовани крррелягрга между избыточным сдвигом ИК-полооы поглощения в избыточной свободной анергией смешения. [30]
Страницы: 1 2 3