Сравнение - подвижность
Cтраница 1
Сравнение подвижности и, обусловленной рассеянием на нейтральных примесях, выделенной из приведенной формулы, с рассчитанной по Эргинсою [6] дает сильно заниженные ее значения. [1]
Сравнение подвижности галоидов может быть продемонстрировано на отношнии веществ к воде при кипячении. В разных пробирках одновременно кипятят с водой хлорбензол и хлористый бензил. [2]
Сравнение подвижности ионов позволяет оценить природу их связи с кислородом, а следовательно, и поведение при протекании реакций с участием расплава. [3]
При сравнении подвижностей бикарбонатов и метакарбо-натов в растворе оказалось, что подвижность последних примерно на 60 % выше. Можно предполагать, что метакарбо-наты отличаются более высокой подвижностью и в мембране, а следовательно, отличаются более высоким прониканием. [4]
Четкую картину для сравнения подвижности атома хлора в г-хлорпропилсульфидах с другими хлорсульфидами и эфирами дают исследования скорости гидролиза в растворе вода - диоксан, проведенные Беме и Седлом [ СЬет. [5]
Другой способ проверки применения уравнений ( 22) и ( 23) к частицам сферической формы состоит в сравнении электроосмотической подвижности и0 с электрофоретической подвижностью ие. [6]
Тот факт, что с увеличением количества присоединенных молекул воды увеличивается объем, а тем самым и трение, подвижность же уменьшается, явствует из сравнения подвижностей К, На, Li с данными таблицы на странице 67, согласно которой степень гидратации в том же порядке сильно возрастает. Вследствие этого обстоятельства ион с наименьшим атомным весом и, казалось бы, с наименьшим объемом, показывает все же самую малую подвижность. [7]
Два типа сравнения скоростей для ряда типичных нуклеофильных замещений в ароматическом ряду показали, что на общие скорости реакций не влияют фак; торы, связанные с разрывом связей. Первый тип включает сравнение подвижности галогенов. Для реакций, о которых известно, что они включают гетеролиз связи углерод - галоген на стадии, определяющей скорость, таких, как SNl - и 5дг2 - реакции насыщенных алкилгало-генидов [1, 2] и образование дегидробензола из о-гало-генфенил-анионов [8], имеет место следующая последовательность подвижности галогенов: IBrCl F. [8]
Два типа сравнения скоростей для ряда типичных нуклеофильных замещений в ароматическом ряду показали, что на общие скорости реакций не влияют фак торы, связанные с разрывом связей. Первый тип включает сравнение подвижности галогенов. Для реакций, о которых известно, что они включают гетеролиз связи углерод - галоген на стадии, определяющей скорость, таких, как SN - и 5 2-реакции насыщенных алкилгало-генидов [1, 2] и образование дегидробензола из о-гало-генфенил-анионов [8], имеет место следующая последовательность подвижности галогенов: I Вг 1 F. [9]
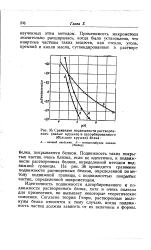 |
Сравнение подвижности растворенного ( малые кружки и адсорбированного ( большие кружки белка. [10] |
Подвижность таких покрытых частиц очень близка, если не идентична, к подвижности растворенных белков, определенной методом подвижной границы. На рис. 36 приводится сравнение подвижности растворенных белков, определенной по методу подвижкой границы, с подвижностью покрщшх частиц, определенной микрометодом. [11]
 |
Седиментационные диаграммы нативной каталазы ( а и сукцини-лированной каталазы ( б. [12] |
Данный метод основан на предположении, что разделение белков в полиакриламидном геле зависит не только от заряда, но в значительной степени и от размера молекул. Установлено соотношение между электрофоретической подвижностью и молекулярным весом различных белков. Сравнение подвижности исследуемой полипептидной цепи с подвижностями белков-маркеров дает молекулярный вес этой цепи. Кроме того, элек-трофоретическая подвижность зависит от количества метилен-бисакриламида, взятого для приготовления геля. [13]
Но быть физически сильнее еще не означает, стать победителем. Более шустрый противник может добиться лучших практических результатов за счет скорости ударов. Отсюда встает необходимость расчета и сравнения подвижности партий. [14]
В работах [46, 47] на основании анализа литературных данных о температурной зависимости активности воды в растворах различных электролитов проводится прямая связь между гидратацией стехиометрической смеси ионов в растворе и изменением активности с температурой. Для характеристики ближней сольватации О.Я. Самойловым [48] введены понятия о положительной и отрицательной сольватации. Таким образом, критерий г / т0 является мерой сравнения подвижности молекул растворителя в растворе и чистом растворителе и определяет тип сольватации ионов в растворе при данной температуре. Случай т / т0 1 соответствует положительной сольватации ионов, а т / г0 1 - отрицательной сольватации. [15]
Страницы: 1 2