Сравнение - вещество
Cтраница 1
Сравнение веществ I, II и III с 2 2 -динитро -, 2 2 -диамино-и 2 2 -дигалогенодифенилами показывает, что относительные места указанных субституентов меняются одинаково. [1]
Для сравнения веществ различного химического состава необходимо рассмотреть теплоту испарения единицы массы вещества при постоянном давлении. [3]
При сравнении веществ 3 и 9 можно отметить, что наличие метиленовой группы, отделяющей фенил от азота, увеличивает фи-тотоксичность вещества. [4]
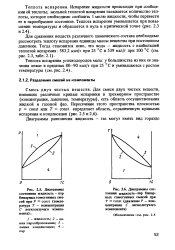
Таким образом, сравнение веществ с разной степенью компактности структуры в твердом и жидком состояниях показывает, что предкристал-лизационные явления развиты у тех из них, у которых структуры ближнего порядка в твердом и жидком состояниях резко различаются. [5]
Температуру самовоспламенения твердых веществ учитывают при сравнении веществ друг с другом, экспертизе причин пожаров и в других случаях. [6]
Растворяют в воде нужное количество выбранного для сравнения вещества. Рекомендуется растворить 1 гЗ 5-дихлорфенола в 100 мл воды. [7]
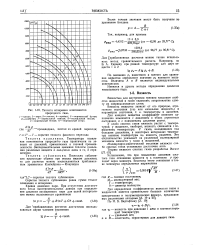 |
Теплота испарения компонентов природного газа. [8] |
По значению р известного и взятого для сравнения вещества определяют значение рг искомого вещества. Величины А и В являются индивидуальными константами. [9]
 |
Изотонический раствор. [10] |
Растворяют в воде нужное количество выбранного для сравнения вещества. Рекомендуется растворить 1 г 3 5-дихлорфенола в 100 см3 воды. [11]
Таким образом, при равных давлениях мольные объемы сухого насыщенного пара приблизительно пропорциональны нормальным температурам кипения, что подтверждается даже при сравнении разнородных веществ. [12]
Температурный интервал существования углеводородов в жидком состоянии различен и изменяется от гомолога к гомологу. Вследствие этого сравнение веществ одного гомологического ряда целесообразно проводить при одинаковых приведенных температурах т Т / ТКИЦ, равных определенным долям от одной соответственной температуры. [13]
Выбор методики исследования в современных условиях представляет нелегкую задачу. Значения, получаемые различными методами, иногда настолько сильно различаются, что сравнение веществ и использование параметров на практике становится просто невозможным. [14]
В 1892 г. на Международном конгрессе в Женезе была принята Женевская номенклатура, теоретическим фундаментом которой явилась теория химического строения. Женевские названия непосредственно выражают строение, не прибегая ( как это происходит в рациональной номенклатуре) к сравнению называемого вещества с более простым прототипом. Женевские названия описывают углеродный скелет органического соединения и содержат указания относительно природы, числа и расположения заместителей, имеющихся в этом скелете. Обозначение углеродного скелета дает основу названия, наличие кратных связей и заместителей отражается в виде дополняющих основу суффиксов и префиксов. Любое органическое соединение при таком подходе оказывается замещенным углеводородом: номенклатуру такого типа можно назвать заместительной. [15]
Страницы: 1 2