Сравнение - теплота - образование
Cтраница 1
Сравнение теплот образования Э2О3 показывает, что наименьшими их значениями характеризуются оксиды лантана и европия. В то же время энтальпия образования оксида европия практически равна таковой для А12О3, а оксида лантана более чем на 100 Дж / моль ее превосходит. Кроме того, энергии активации оксидирования, как правило, столь малы, что многие из РЗЭ неустойчивы уже при обычных условиях. Лантан например, хранят в бензоле во избежание окисления на воздухе. [1]
 |
Внутренняя периодичность. [2] |
Сравнение теплот образования Э Оз показывает, что наименьшими их значениями характеризуются оксиды лантана и европия. В то же время энтальпии образования оксида европия практически равна таковой для А Оз, а оксида лантана более чем на 100 Дж / моль ее превосходит. Таким образом, среди характеристических оксидов лантаноидов наименьшей прочностью отличается оксид европия, хотя он сам по себе относится к категории таких прочных соединений, как АЬОз. Кроме того, энергии активации оксидирования, как правило, столь малы, что многие из РЗЭ неустойчивы уже при обычных условиях. Лантан, например, хранят в бензоле во избежание окисления на воздухе. [3]
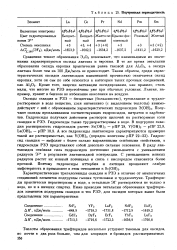 |
Внутренняя периодичность. [4] |
Сравнение теплот образования Э2Оз показывает, что наименьшими их значениями характеризуются оксиды лантана и европия. В то же время энтальпии образования оксида европия практически равна таковой для А12О3, а оксида лантана более чем На 100 Дж / моль ее превосходит. Таким образом, среди характеристических оксидов лантаноидов наименьшей прочностью отличается оксид европия, хотя он сам по себе относится к категории таких прочных соединений, как А12Оз - Кроме того, энергии активации оксидирования, как правило, столь малы, что многие из РЗЭ неустойчивы уже при обычных условиях. Лантан, например, хранят в бензоле во избежание окисления на воздухе. [5]
Сравнение теплот образования воды и сероводорода и энергии связей водорода с кислородом и серой ( ДЯн2о 57 8 ккал, A H2s - 4 8 ккал и энергия связи Н - ОН 116 ккал, а Н - S - Н 90 ккал) свидетельствуют о значительно меньшей химической активности серы по сравнению с кислородом. Смесь паров серы с водородом не взрывается, как смесь водорода с кислородом. Синтез сероводорода из элементов - обратимый процесс и ограничен, следовательно, равновесным состоянием, тогда как вода практически не диссоциирует даже при очень высоких температурах. [6]
Сравнение теплот образования воды и сероводорода и энергии связей водорода с кислородом и серой ( ДНн2о 57 8 ккал, А н 5 - 4 8 ккал и энергия связи Н - ОН 116 ккал, а Н - S - Н 90 ккал) свидетельствуют о значительно меньшей химической активности серы по сравнению с кислородом. Смесь паров серы с водородом не взрывается, как смесь водорода с кислородом. Синтез сероводорода из элементов - обратимый процесс и ограничен, следовательно, равновесным состоянием, тогда как вода практически не диссоциирует даже при очень высоких температурах. [7]
На рис. 178 приведено сравнение теплот образования фторидов и окислов атомов 2-го периода. [8]
Второй метод оценки энергии мезомерии состоит в сравнении теплот образования, выведенных из теплот сгорания с суммой энергий связей. Единственным соединением, для которого требуется введение большой поправки в полученную вышеуказанным способом энергию мезомерии, является дифенилен. [9]
Значение теплоты образования Р4О6 может быть оценено путем сравнения теплот образования окислов элементов - аналогов фосфора. [10]
Степень прочности связи разных галогенов с углеродом выявляется также при сравнении теплот образования ( стр. [11]
Сходная величина разности энтальпий ( 4 79 0 94 ккал / молъ) была получена из сравнения теплот образования транс-син-транс-к траис-актпи-тпран-с - пергидроантраценов. [12]
Кроме них в таблице приводятся данные для серии комплексных аммиакатов и аминатов, вычисленные на основании сравнения теплот образования соответствующих гало-генидов. [13]
При наличии нескольких смежных кратных связей дополнительная энергия незначительно уменьшается за счет энергии резонанса. Однако, как показывает сравнение теплот образования бутана, бутадиена, винилацетилена и диацетилена ( см. табл. 1), содержание энергии в этих соединениях все же больше, чем в насыщенных углеводородах. [14]
Для вычисления энергии делокализации из экспериментальных данных обычно используют один из двух методов. Второй метод основан на сравнении теплоты образования, вычисленной из теплоты сгорания, с теплотой образования, полученной суммированием энергий связей. Разность вычисленных таким образом теплот образования дает экспериментальную оценку теплоты делокализации. [15]
Страницы: 1 2