Сравнение - активность - катализатор
Cтраница 1
Сравнение активности катализаторов на модельных водных растворах сульфида натрия в вышеописанных условиях показало, что при окислении стоков, содержащих только сульфидную серу, катализаторы УВКО и ТИКОС являются несколько более активными, чем КС-2, хотя это различие невелико. [1]
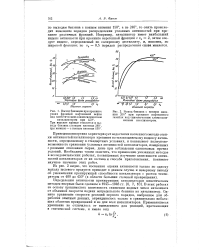
Сравнение активности окиспомолибденовых катализаторов с известной удельной поверхностью показало что активность их увеличивается с повышением концентрации молибдена до покрытия всей поверхности окиси алюминия приблизительно мономолекулярным слоем активного окисла. После достижения этой точки активность остается практически постоянной. [2]
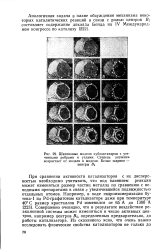 |
Шариковые модели кубооктаэдров с усеченными ребрами и углами. Степень усечения возрастает от модели к модели. Белые шарики - центры 55. [3] |
При сравнении активности катализаторов с их дисперсностью необходимо учитывать, что под влиянием реакции может изменяться размер частиц металла по сравнению с исходными препаратами в связи с увеличившейся подвижностью отдельных атомов. Совершенно очевидно, что в результате воздействия реакционной системы может измениться и число активных центров, например центров БЗ, определенных предварительно, до работы катализатора. [4]
Приведенная картина характеризует недостатки косвенного метода оценки активностей катализатора крекинга по так называемому индексу активности, определяемому в стандартных условиях, и показывает полную невозможность сравнения условных активностей катализаторов, измеренных с разными эталонами сырья, даже при соблюдении одинаковых прочих условий. [5]
Приведенная картина характеризует не достатки косвенного метода оценки активностей катализатора крекинга по так называемому индексу активности, определяемому в стандартных условиях, и показывает полную невозможность сравнения условных активностей катализаторов, измеренных с разными эталонами сырья, даже при соблюдении одинаковых прочих условий. Необходимо также заметить, что применение указанных методов в исследовательских работах, посвященных изучению зависимости активностей катализаторов от их состава и способа приготовления, понижает научное значение этих работ. [7]
В работах [214, 215] сделана попытка сопоставить некоторые структурные свойства катализаторов Ni - MgO, Ni - А12Оз, Ni - ZnO и Ni - Cr2O3 с их активностью в реакции деметили-рования толуола под влиянием водяного пара. К сожалению, неправильное сравнение активностей катализаторов ( % превращения на м2 Ni) делает эту задачу невозможной. [8]
Однако следует указать, что при определении активности импульсным микрометодом находится величина, пропорци - опальная произведению истинной константы скорости и константы адсорбционного равновесия. Таким образом, при сравнении активности катализаторов, найденной этим мето - - дом, не учитывается вклад адсорбционного взаимодействия. Если исключить последний и сравнивать истинные константы скорости, которые являются наиболее строгими характеристиками каталитической активности, то различие между исследованными образцами оказывается сравнительно небольшим. Ниже приводятся значения истинных констант скорости реакции крекинга кумола ( при 436 С), полученных при исследовании кинетики дифференциальным методом, а также истинных энергий активации для лантанового, кальциевого и декатионирован ного образцов. [9]
На практике часто пользуются понятием производительность катализатора, под которой подразумевают количество данного продукта, образующегося в единицу времени на единице объема катализатора. Величина производительности, хоть и достаточна иногда для практического сравнения активности катализаторов, однако имеет следующий недостаток: она характеризует суммарно и каталитическую активность вещества, и его удельную поверхность. Поэтому, имея такие величины для разных катализаторов, нельзя установить, почему один катализатор активнее другого: потому ли, что активнее его поверхность, или потому, что он более порист, обладает более развитой поверхностью. [10]
Изложенный метод был использован авторами ( 21 - 22J для крекинга олефиновых, нафтеновых, ароматических углеводородов и фракции 260 - 316 С восточно-техасской нефти. Методика проведения опытов и расчета полученных данных аналогична вьслеописанной. Сравнение активности катализаторов крекинга также проводится по константе скорости реакции в заданных условиях. [11]
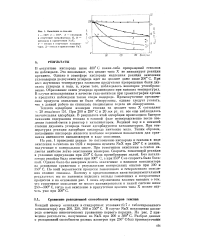 |
Окисление - гексана. [12] |
Водяной пар и в меньшей степени двуокись углерода также адсорбируются катализатором. При температурах реакции адсорбция кислорода ничтожно мала. Таким образом, поглощение кислорода является наиболее надежным показателем для сравнения активности катализаторов в ходе окисления. [13]
Страницы: 1